题目内容
12.下列物质转化在给定条件下不能实现的是( )| A. | ${Fe}_{2}{O}_{3}\stackrel{HCl(aq)}{→}{FeCl}_{3}(aq)\stackrel{△}{→}{Fe(OH)}_{3}(胶体)$ | |
| B. | ${Al}_{2}{O}_{3}\stackrel{NaOH(aq)}{→}{NaAlO}_{2}(aq)\stackrel{HCl(aq)}{→}{AlCl}_{3}$ | |
| C. | ${MgCl}_{2}(aq)\stackrel{石灰乳}{→}Mg{(OH)}_{2}\stackrel{煅烧}{→}MgO$ | |
| D. | $Fe{S}_{2}\stackrel{煅烧}{→}{SO}_{3}\stackrel{{H}_{2}O}{→}{H}_{2}{SO}_{4}$ |
分析 A.氧化铁和盐酸反应生成氯化铁,氯化铁溶液中加入氢氧化钠溶液生成氢氧化铁沉淀;
B.氧化铝溶于氢氧化钠溶液生成偏铝酸钠,偏铝酸钠溶液中加入过量的盐酸反应生成氯化铝;
C.氯化镁溶液中加入石灰乳生成氢氧化镁沉淀,氢氧化镁受热分解生成氧化镁;
D.FeS2煅烧生成二氧化硫和氧化铁,不能一步生成三氧化硫.
解答 解:A.氧化铁和盐酸反应生成氯化铁,Fe2O3+6HCl=2FeCl3+3H2O,氯化铁溶液中加入氢氧化钠溶液生成氢氧化铁沉淀,FeCl3+3NaOH=Fe(OH)3↓+3NaCl,能实现转化关系,故A不符合;
B.氧化铝溶于氢氧化钠溶液生成偏铝酸钠,Al2O3+2NaOH=2NaAlO2+H2O,偏铝酸钠溶液中加入过量的盐酸反应生成氯化铝,NaAlO2+4HCl=NaCl+AlCl3+H2O,能实现转化关系,故B不符合;
C.氯化镁溶液中加入石灰乳生成氢氧化镁沉淀,MgCl2+Ca(OH)2=Mg(OH)2↓+CaCl2,氢氧化镁受热分解生成氧化镁,Mg(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$MgO+H2O,能实现转化关系,故C不符合;
D.FeS2煅烧生成二氧化硫和氧化铁,4FeS2+11O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+8SO2,不能一步生成三氧化硫,不能实现转化关系,故D符合;
故选D.
点评 本题考查了铁、铝及其化合物性质的理解应用,主要是反应过程和产物生成的判断,掌握基础是关键,题目较简单.

练习册系列答案
相关题目
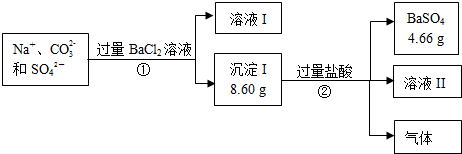
2.今有一混合物的水溶液,只可能含有以下离子中的若干种:Na+、Ba2+、Cl-、CO32-、SO42-,现取200mL溶液加足量BaCl2溶液后,得干燥沉淀12.54g,经足量盐酸洗涤、干燥后,沉淀质量为4.66g,根据上述实验,以下推测正确的是( )
| A. | 可能存在大量Ba2+ | B. | 溶液中Na+物质的量小于0.12mol | ||
| C. | 可能存在Cl- | D. | 溶液中c(Na+)≥0.6mol•L-1 |
3.下列各个选项中的转化,不能一步完成的是( )
| A. | Na→NaOH→Na2CO3 | B. | NaCl→Cl2→Fe Cl3 | ||
| C. | CO→CO2→C | D. | Al2O3→Al(OH)3→AlCl3 |
20.下列关于化学键的说法正确的是( )
| A. | 原子间的相互作用都是化学键 | |
| B. | 相邻的两个原子间一定能形成化学键 | |
| C. | 化学键就是相邻的两个原子间的吸引作用 | |
| D. | 化学键包括相邻的两个原子间的吸引和排斥两方面的强烈作用 |
4.下列离子方程式书写正确的是( )
| A. | 铜跟硝酸银溶液反应:Cu+Ag+═Cu2++Ag | |
| B. | 稀硫酸与氢氧化钡溶液混合:SO42-+Ba2+═BaSO4↓ | |
| C. | 碳酸钙与醋酸反应:CaCO3+2H+═Ca2++CO2↑+H2O | |
| D. | 盐酸与澄清石灰水反应:H++OH-═H2O |
2.控制适宜的条件,将反应2Fe3++2Iˉ?2Fe2++I2设计成如图所示的原电池.下列判断 错误的是( )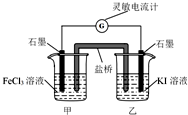

| A. | 反应开始时,乙中石墨电极上发生氧化反应 | |
| B. | 反应开始时,甲中石墨电极为正极 | |
| C. | 电流计读数为零时,反应达到化学平衡状态 | |
| D. | 电流计读数为零后,在甲中溶入FeCl2固体,乙中石墨电极为负极 |