题目内容
下列叙述正确的是( )
| A、由水电离出的c(H+)=10-5mol/L的溶液中的溶质可能是氯化铵,也可能是碳酸钠 |
| B、室温下,向0.01 mol?L-1NH4HSO4溶液中滴加烧碱NaOH溶液至中性,则溶液中的离子浓度关系为c(Na+)=c(SO42-)>c(NH4+)>c(OH-)=c(H+) |
| C、pH=5的CH3COOH溶液和pH=5的NH4Cl溶液加水稀释后,恢复至原温度,c(OH-)均减小 |
| D、25℃时,pH=4.75、浓度均为0.1 mol?L-1的CH3COOH、CH3COONa混合溶液:c(CH3COO-)+c(OH-)<c(CH3COOH)+c(H+) |
考点:离子浓度大小的比较,弱电解质在水溶液中的电离平衡,水的电离,盐类水解的应用
专题:基本概念与基本理论
分析:A.酸或碱抑制水电离,含有弱离子的盐溶液促进水电离;
B.如果二者以1:1反应,溶液中的溶质是硫酸钠、硫酸铵,溶液呈酸性,要使混合溶液呈中性,则n(NH4HSO4):n(NaOH)<1:1,再结合物料守恒、电荷守恒判断;
C.加水稀释促进弱电解质电离、弱离子水解,但这两种溶液的酸性都减弱;
D.pH=4.75、浓度均为0.1 mol?L-1的CH3COOH、CH3COONa混合溶液呈酸性,CH3COOH的电离程度大于CH3COO-的水解程度,结合电荷守恒解答.
B.如果二者以1:1反应,溶液中的溶质是硫酸钠、硫酸铵,溶液呈酸性,要使混合溶液呈中性,则n(NH4HSO4):n(NaOH)<1:1,再结合物料守恒、电荷守恒判断;
C.加水稀释促进弱电解质电离、弱离子水解,但这两种溶液的酸性都减弱;
D.pH=4.75、浓度均为0.1 mol?L-1的CH3COOH、CH3COONa混合溶液呈酸性,CH3COOH的电离程度大于CH3COO-的水解程度,结合电荷守恒解答.
解答:
解:A.酸或碱抑制水电离,含有弱离子的盐溶液促进水电离,由水电离出的c(H+)=10-5mol/L>10-7mol/L,则该溶液的溶质为含有弱离子的盐,所以溶液中的溶质可能是氯化铵,也可能是碳酸钠,故A正确;
B.如果二者以1:1反应,溶液中的溶质是硫酸钠、硫酸铵,溶液呈酸性,要使混合溶液呈中性,则n(NH4HSO4):n(NaOH)<1:1,根据物料守恒得c(Na+)>c(SO42-),根据电荷守恒得c(Na+)+c(NH4+)=2c(SO42-),所以c(SO42-)>c(NH4+),故B错误;
C.加水稀释促进弱电解质电离、弱离子水解,但这两种溶液的酸性都减弱,所以c(OH-)均增大,故C错误;
D.pH=4.75、浓度均为0.1 mol?L-1的CH3COOH、CH3COONa混合溶液呈酸性,CH3COOH的电离程度大于CH3COO-的水解程度,根据电荷守恒得c(CH3COO-)+c(OH-)=c(Na+)+c(H+),因为CH3COOH的电离程度大于CH3COO-的水解程度,所以c(CH3COOH)<c(Na+),则c(CH3COO-)+c(OH-)>c(CH3COOH)+c(H+),故D错误;
故选A.
B.如果二者以1:1反应,溶液中的溶质是硫酸钠、硫酸铵,溶液呈酸性,要使混合溶液呈中性,则n(NH4HSO4):n(NaOH)<1:1,根据物料守恒得c(Na+)>c(SO42-),根据电荷守恒得c(Na+)+c(NH4+)=2c(SO42-),所以c(SO42-)>c(NH4+),故B错误;
C.加水稀释促进弱电解质电离、弱离子水解,但这两种溶液的酸性都减弱,所以c(OH-)均增大,故C错误;
D.pH=4.75、浓度均为0.1 mol?L-1的CH3COOH、CH3COONa混合溶液呈酸性,CH3COOH的电离程度大于CH3COO-的水解程度,根据电荷守恒得c(CH3COO-)+c(OH-)=c(Na+)+c(H+),因为CH3COOH的电离程度大于CH3COO-的水解程度,所以c(CH3COOH)<c(Na+),则c(CH3COO-)+c(OH-)>c(CH3COOH)+c(H+),故D错误;
故选A.
点评:本题考查了离子浓度大小比较,根据溶液中的溶质及溶液酸碱性再结合电荷守恒、物料守恒来分析解答,易错选项是B,题目难度中等.

练习册系列答案
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案
相关题目
下列化学用语正确的是( )
A、S原子的结构示意图: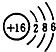 |
B、氯化钠的电子式: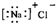 |
| C、乙烯的结构简式:CH2=CH2 |
| D、碳酸钠的电离方程式:NaHCO3=Na++H++CO32- |
下列物质能发生消去反应的是( )
| A、CH3I |
| B、CH3OH |
| C、(CH3)3COH |
| D、(CH3)3C-CH2C1 |
在40GPa高压下,用激光器加热到1 800K时,人们成功制得了原子晶体干冰,下列推断错误的是( )
| A、原子晶体干冰有很高的熔、沸点,有很大的硬度 |
| B、原子晶体干冰易气化,可用作致冷剂 |
| C、原子晶体干冰硬度大,可用于耐磨材料 |
| D、每摩原子晶体干冰中含4mol C-O键 |
下列反应的离子方程式正确的是( )
| A、澄清石灰水跟盐酸反应:OH-+H+=H2O |
| B、金属钠跟水反应:Na+2H2O=Na++2OH-+H2↑ |
| C、碳酸钡与醋酸反应:BaCO3+2H+=CO2↑+Ba2++H2O |
| D、碳酸氢钠溶液和氢氧化钠溶液反应:HCO3-+OH-=CO2↑+H2O |
浅绿色的Fe(NO3)2溶液中逐滴加入少量稀盐酸时,溶液的颜色变化是( )
| A、变浅 | B、变为红色 |
| C、没有变化 | D、变为黄色 |
化学实验中安全意识是重要的科学素养,下列实验操作正确的是( )
| A、将含硫酸的废液倒入水槽,用水冲入下水道 |
| B、做氢气还原氧化铜实验时,先通氢气再加热 |
| C、配制稀硫酸时,可先在量筒中加一定体积的水,再边搅拌边慢慢加入浓硫酸 |
| D、点燃酒精灯时可以拿燃着的酒精灯引燃另一只酒精灯 |
下列各组离子能在指定的环境下可以大量共存的是( )
| A、在pH=0的溶液中:Na+、Fe2+、Cl-、NO3- |
| B、由水电离出的c(H+)=1×10-14mol?L-1的溶液:K+、NH4+、Cl-、CO32- |
| C、c(H+)<c(OH-)溶液:Na+、K+、SO32-、AlO2- |
| D、某无色透明溶液:Na+、Al3+、SO42-、HCO3- |
最近全国各大城市出现雾埋天气较多,加强环境的保护有利国民的健康,下列做法不能体现低碳生活的是( )
| A、减少食物加工过程 |
| B、注意节约用电 |
| C、尽量购买本地的、当季的食物 |
| D、大量使用薪柴为燃料 |