题目内容
下列比较中正确的是( )
| A、离子还原性:S2->Cl->Br->I- | B、氧化性:F2>Cl2>Br2 | C、酸性:H2SO4>HClO4>H3PO4 | D、非金属性:F>Cl>S>O |
分析:A.元素的非金属性越强,对应阴离子的还原性越弱;
B.元素的非金属性越强,单质的氧化性越强;
C.元素的非金属性越强,最高价氧化物对应的水化物的酸性越强;
D.同主族元素,电子层数越多,非金属性越弱,同周期原子序数越大,非金属性越强.
B.元素的非金属性越强,单质的氧化性越强;
C.元素的非金属性越强,最高价氧化物对应的水化物的酸性越强;
D.同主族元素,电子层数越多,非金属性越弱,同周期原子序数越大,非金属性越强.
解答:解:A.非金属性:Cl>Br>I>S,元素的非金属性越强,对应阴离子的还原性越弱,所以离子还原性:S2->I->Br->Cl-,故A错误;
B.非金属性:F>Cl>Br,元素的非金属性越强,单质的氧化性越强,所以单质的氧化性为:F2>Cl2>Br2,故B正确;
C.非金属性:Cl>S>P,元素的非金属性越强,最高价氧化物对应的水化物的酸性越强,所以酸性:HClO4>H2SO4>H3PO4,故C错误;
D.同主族元素,电子层数越多,非金属性越弱,同周期原子序数越大,非金属性越强,则非金属性:F>O>Cl>S,故D错误;
故选:B.
B.非金属性:F>Cl>Br,元素的非金属性越强,单质的氧化性越强,所以单质的氧化性为:F2>Cl2>Br2,故B正确;
C.非金属性:Cl>S>P,元素的非金属性越强,最高价氧化物对应的水化物的酸性越强,所以酸性:HClO4>H2SO4>H3PO4,故C错误;
D.同主族元素,电子层数越多,非金属性越弱,同周期原子序数越大,非金属性越强,则非金属性:F>O>Cl>S,故D错误;
故选:B.
点评:本题考查非金属元素的性质,明确同周期、同主族元素的性质变化规律及元素非金属性的比较方法是解答本题的关键,难度不大.

练习册系列答案
相关题目
a、b、c、d是四种短周期元素.a、b、d同周期,c、d同主族.a的原子结构示意图为 ,b与c形成化合物的电子式为
,b与c形成化合物的电子式为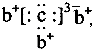 下列比较中正确的是( )
下列比较中正确的是( )
 ,b与c形成化合物的电子式为
,b与c形成化合物的电子式为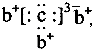 下列比较中正确的是( )
下列比较中正确的是( )| A、原子半径:a>c>d>b | B、最高价含氧酸的酸性c>d>a | C、原子序数:a>d>b>c | D、单质的氧化性a>b>d>c |
 ,b与c形成化合物的电子式为
,b与c形成化合物的电子式为 .下列比较中正确的是( )
.下列比较中正确的是( )