题目内容
12.把a、b、c、d四块金属片浸泡在稀硫酸中,用导线两两相连可以组成各种原电池.若a、b相连时,a为负极;c、d相连时,d上有气泡逸出;a、c相连时,a极减轻;b、d相连时,b为正极.则这四种金属活泼性顺序由强到弱的顺序为( )| A. | a>b>c>d | B. | a>c>b>d | C. | a>c>d>b | D. | b>d>a>c |
分析 原电池中,负极材料为较活泼的金属,发生氧化反应,正极为较不活泼的金属,发生还原反应,以此判断金属的活动性.
解答 解:若a.b相连时,a为负极,活动性a>b;
c、d相连时,d上有气泡逸出,所以d为正极,c为负极,活动性c>d;
a.c相连a极减轻,a为负极,c为正极,活动性a>c;
b.d相连时b为正极,d为负极,活动性d>b;
则有活动性a>c>d>b.
故选C.
点评 本题考查金属活动性的比较,题目难度不大,注意金属活动性的比较方法的积累.

练习册系列答案
相关题目
2.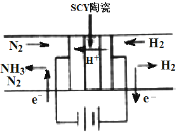 科学家采用高质子导电性的SCY陶瓷交换膜为质子导体,可以实现在低温常压条件下电化学方法合成氨,该方法N2和H2的转化率远高于现在工业上使用的氨合成法.其实验原理如图所示.下列关于电化学合成氨的叙述不正确的是( )
科学家采用高质子导电性的SCY陶瓷交换膜为质子导体,可以实现在低温常压条件下电化学方法合成氨,该方法N2和H2的转化率远高于现在工业上使用的氨合成法.其实验原理如图所示.下列关于电化学合成氨的叙述不正确的是( )
 科学家采用高质子导电性的SCY陶瓷交换膜为质子导体,可以实现在低温常压条件下电化学方法合成氨,该方法N2和H2的转化率远高于现在工业上使用的氨合成法.其实验原理如图所示.下列关于电化学合成氨的叙述不正确的是( )
科学家采用高质子导电性的SCY陶瓷交换膜为质子导体,可以实现在低温常压条件下电化学方法合成氨,该方法N2和H2的转化率远高于现在工业上使用的氨合成法.其实验原理如图所示.下列关于电化学合成氨的叙述不正确的是( )| A. | 阴极的电极反应是N2+6H++6e-=2NH3 | |
| B. | 阴极材料和阳极材料都可选用铁 | |
| C. | H2在阳极上发生反应是H2-2e-=2H+ | |
| D. | 该过程的总反应式是N2+3H2$\frac{\underline{\;电解\;}}{\;}$2NH3 |
3. 有机物的结构简式如图:则此有机物可发生的反应类型有( )
有机物的结构简式如图:则此有机物可发生的反应类型有( )
①取代 ②加成 ③消去 ④酯化 ⑤水解 ⑥氧化 ⑦中和 ⑧还原.
 有机物的结构简式如图:则此有机物可发生的反应类型有( )
有机物的结构简式如图:则此有机物可发生的反应类型有( )①取代 ②加成 ③消去 ④酯化 ⑤水解 ⑥氧化 ⑦中和 ⑧还原.
| A. | ①②③⑤⑥⑧ | B. | ②③④⑤⑥ | C. | ②③④⑤⑥⑦ | D. | ①②③④⑤⑥⑦⑧ |
7.我国科学家首次合成了一种过渡金属的新核素${\;}_{72}^{185}$Hf,其单质有延展性、不易被腐蚀等特点,可应用于高科技领域.185Hf可由180Hf转化而成,下列有关180Hf、185Hf说法正确的是( )
| A. | 180Hf转化为185Hf是化学变化 | |
| B. | 二者的核外电子数分别为108、113 | |
| C. | 1mol 180Hf的中子数比1mol 185Hf少5NA | |
| D. | 在元素周期表中的位置不同 |
17.用括号内试剂除去下列各物质中的少量杂质,正确的是( )
| A. | 溴苯中的溴(苯) | B. | 甲烷中的乙烯(溴水) | ||
| C. | 乙醇中的水(金属钠) | D. | 甲烷中的乙烯(酸性高锰酸钾溶液) |
4.根据表中信息判断,下列选项不正确的是( )
| 序号 | 反应物 | 产物 |
| ① | KMnO4、H2O2、H2SO4 | K2SO4、MnSO4 |
| ② | Cl2、FeBr2 | FeCl3、FeBr3 |
| ③ | MnO4- | Cl2、Mn2+ |
| A. | 第①组反应的其余产物为H2O和 O2 | |
| B. | 第②组反应中参加反应的Cl2与 FeBr2的物质的量之比为1:2 | |
| C. | 第③组反应中生成1 mol Cl2,转移电子2 mol | |
| D. | 氧化性由强到弱顺序为MnO4->Cl2>Fe3+>Br2 |
1.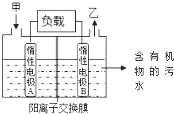 一种处理污水的燃料电池模型如图所示.该电池工作时,只需把污水注入反应池,细菌就可将污水中的有机物分解,在此过程中释放出电子、质子和乙.下列叙述不正确的是( )
一种处理污水的燃料电池模型如图所示.该电池工作时,只需把污水注入反应池,细菌就可将污水中的有机物分解,在此过程中释放出电子、质子和乙.下列叙述不正确的是( )
 一种处理污水的燃料电池模型如图所示.该电池工作时,只需把污水注入反应池,细菌就可将污水中的有机物分解,在此过程中释放出电子、质子和乙.下列叙述不正确的是( )
一种处理污水的燃料电池模型如图所示.该电池工作时,只需把污水注入反应池,细菌就可将污水中的有机物分解,在此过程中释放出电子、质子和乙.下列叙述不正确的是( )| A. | B电极为正极 | |
| B. | 气体乙可能为CO2 | |
| C. | O2在A电极得电子 | |
| D. | 电池工作时,B电极附近的pH逐渐减小 |
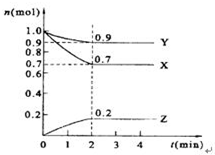 某温度时,在2L的密闭容器中,X、Y、Z三种物质的量随时间的变化曲线如图所示.
某温度时,在2L的密闭容器中,X、Y、Z三种物质的量随时间的变化曲线如图所示.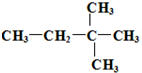 由另一种烃D通过加成反应而制得,则烃D的可能的是
由另一种烃D通过加成反应而制得,则烃D的可能的是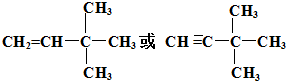 (任写一种可能的结构简式)
(任写一种可能的结构简式)