题目内容
10克Fe2O3、SiO2、Al2O3混合物加入足量的100 mL x mol/L稀硫酸中,过滤,然后加入10 mol/L NaOH溶液,产生沉淀的质量和加入NaOH溶液体积如图。以下叙述错误的是

A.滤出的物质为SiO2
B.可求出x的值
C.可求出Al2O3的质量分数
D.可求出Fe2O3的质量分数
D
【解析】
试题分析:A、二氧化硅是酸性氧化物,与硫酸不反应,则滤出的物质为SiO2,A正确;B、滤液中含有硫酸铝、硫酸铁和硫酸,根据图像可知当加入NaOH100mL时沉淀达到最大值,可知沉淀为氢氧化铁和氢氧化铝,溶液中溶质为硫酸钠,根据原子守恒可知H2SO4~Na2SO4~2NaOH,则n(Na)=2n(硫酸),据此可计算x的值,B正确;C、根据图像可知加入NaOH110mL时,氢氧化铝全部溶解,即溶解氢氧化铝消耗的氢氧化钠是10ml,则根据方程式Al(OH)3+NaOH=NaAlO2+2H2O可计算氢氧化铝的物质的量,进而计算Al2O3的质量分数,C正确;D、由于滤液中过量的硫酸的量和沉淀的总质量未知,因此不能计算氧化铁的质量,则不能计算氧化铁的质量分数,D错误,答案选D。
考点:考查混合物计算的有关图像分析

选考题【化学一一选修化学与技术】(15分)以炼锌烟尘(主要成份为ZnO,含少量CuO和FeO)为原料,可以制取氯化锌和金属锌。
Ⅰ、制取氯化锌主要工艺如下:

下表列出了相关金属离子生成氢氧化物沉淀的pH (开始沉淀的pH按金属离子浓度为1.0 mol·L-1计算)。
金属离子 | 开始沉淀的pH | 沉淀完全的pH |
Fe3+ | 1. 1 | 3. 2 |
Zn2+ | 5. 2 | 6. 4 |
Fe2+ | 5. 8 | 8. 8 |
(1)加入H2O2溶液发生反应的离子方程式为 。
(2)流程图中,为了降低溶液的酸度,试剂X不可以是 (选填序号:
a.ZnO;b.Zn(OH)2 ;c.Zn2(OH)2CO3 ;d.ZnSO4;pH应调整到 ;
(3)氯化锌能催化乳酸(2-羟基丙酸)生成丙交酯(C6H8O4)和聚乳酸,丙交酯的结构简式为 ,聚乳酸的结构简式为 ;
Ⅱ、制取金属锌采用碱溶解ZnO(s)+2NaOH(aq)+H2O(l)=Na2[Zn(OH)4](aq),然后电解浸取液。
(4)以石墨作电极电解时,阳极产生的气体为 ;阴极的电极反应为 ;
(5)炼锌烟尘采用碱溶,而不采用酸溶后电解,主要原因是 。

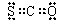
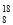 O2-离子结构示意图:
O2-离子结构示意图: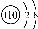
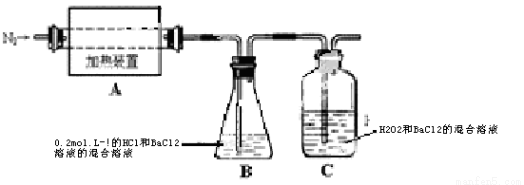
 2Fe2O3?xH2O + 8H+,硫酸亚铁铵 溶液较硫酸亚铁溶液不易被氧气氧化,其原因是 。
2Fe2O3?xH2O + 8H+,硫酸亚铁铵 溶液较硫酸亚铁溶液不易被氧气氧化,其原因是 。