题目内容
5.某二元化合物甲有刺鼻气味,极易被水和酸吸收,是一类重要的火箭燃料.将3.20g甲加热至完全分解,得到一种常见的气体单质和4.48L的H2(已折算成标准状况);已知甲分子内各原子均达到稳定结构.工业上用尿素[CO(NH2)2]投料到按一定比例混合的NaClO与NaOH混合溶液中反应可制得甲,同时得到副产品碳酸钠等物质.(1)写出甲的分子式N2H4.
(2)适量氯气通入NaOH溶液中可以得到上述混合溶液,写出该反应的离子反应方程式:Cl2+2OH-=ClO-+Cl-+H2O.
(3)工业上常用甲使锅炉内壁的铁锈转化为结构较致密的磁性氧化铁(Fe3O4),以减慢锅炉内壁的锈蚀.其化学方程式为N2H4+6Fe2O3=N2↑+4Fe3O4+2H2O.
分析 甲加热至完全分解,得到一种常见的气体单质和4.48L的H2(已折算成标准状况),则甲中含有H元素,工业上用尿素[CO(NH2)2]投料到按一定比例混合的NaClO与NaOH混合溶液中反应可制得甲,同时得到副产品碳酸钠等物质,根据元素守恒可知甲中含有N元素,综上可知,甲中含有N和H两种元素,n(H2)=$\frac{4.48L}{22.4L/mol}$=0.2mol,则m(H)=0.2mol×2×1g/mol=0.4g,则3.20g甲中含有m(N)=3.20g-0.4g=2.8g,n(N)=$\frac{2.8g}{14g/mol}$=0.2mol,所以n(N):n(H)=0.2mol:0.4mol=1:2,甲分子内各原子均达到稳定结构,可知甲为N2H4,据此进行解答.
解答 解:(1)甲加热至完全分解,得到一种常见的气体单质和4.48L的H2(已折算成标准状况),则甲中含有H元素,工业上用尿素[CO(NH2)2]投料到按一定比例混合的NaClO与NaOH混合溶液中反应可制得甲,同时得到副产品碳酸钠等物质,根据元素守恒可知甲中含有N元素,综上可知,甲中含有N和H两种元素,n(H2)=$\frac{4.48L}{22.4L/mol}$=0.2mol,则m(H)=0.2mol×2×1g/mol=0.4g,则3.20g甲中含有m(N)=3.20g-0.4g=2.8g,n(N)=$\frac{2.8g}{14g/mol}$=0.2mol,所以n(N):n(H)=0.2mol:0.4mol=1:2,甲分子内各原子均达到稳定结构可知甲的分子式为N2H4,
故答案为:N2H4;
(2)适量氯气通入NaOH溶液中可以得到上述混合溶液,该反应的离子反应方程式:Cl2+2OH-=ClO-+Cl-+H2O,
故答案为:Cl2+2OH-=ClO-+Cl-+H2O;
(3)工业上常用甲使锅炉内壁的铁锈转化为结构较致密的磁性氧化铁(Fe3O4),以减慢锅炉内壁的锈蚀,Fe元素化合价降低,则N元素被氧化生成氮气,其化学方程式为:N2H4+6Fe2O3=N2↑+4Fe3O4+2H2O,
故答案为:N2H4+6Fe2O3=N2↑+4Fe3O4+2H2O.
点评 本题考查无机物的推断、化学方程式的书写,属于计算型推断,题目难度中等,注意掌握化学方程式的书写原则,试题侧重考查学生分析计算能力及知识的迁移应用能力.

 阅读快车系列答案
阅读快车系列答案| 选项 | 操作 | 现象 | 解释或结论 |
| A | 用容量瓶配制溶液时,定容后摇匀 | 液面低于刻度线 | 浓度一定偏高 |
| B | 燃着的镁条深入盛CO2的集气瓶中 | 镁条继续燃烧 | 镁有比较强的还原性 |
| C | 分别向酸性KMnO4溶液中加入FeCl2或通入SO2 | 酸性KMnO4溶液颜色均褪去 | Fe2+具有还原性,SO2具有漂白性 |
| D | 过量Fe粉加入稀HNO3中,充分反应后,滴入KSCN溶液 | 溶液呈红色 | 稀HNO3将Fe氧化Fe3+ |
| A. | A | B. | B | C. | C | D. | D |
| A. | 平衡向逆反应方向转动 | B. | 平衡不移动 | ||
| C. | C的百分含量增大 | D. | C的百分含量减小 |
| A | B | C | D |
 |  |  |  |
| 使用填埋法处理未经分类的生活垃圾 | 食用油脂能促进人体对某些维生素的吸收 | 利用二氧化碳可制造全降解塑料,有利于缓解温室效应 | 药皂中的少量苯酚,可起到杀菌消毒的作用 |
| A. | A | B. | B | C. | C | D. | D |
| A. | NH3+H3O+═NH${\;}_{4}^{+}$+H2O:NH3结合H+的能力比H2O强 | |
| B. | Al2O3+2NaOH═2NaAlO2+H2O:Al2O3是两性氧化物 | |
| C. | HClO+SO2+H2O═HCl+H2SO4:酸性 HClO>H2SO4 | |
| D. | 已知C(s,石墨)=C(s,金刚石)△H=+1.9 kJ/mol:金刚石比石墨稳定 |
| A. | 导电性 | B. | 水溶性 | C. | 氧化性 | D. | 化学稳定性 |
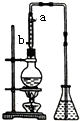 市售乙醛通常为40%左右的乙醛溶液.久置的乙醛溶液会产生分层现象,上层为无色油状液体,下层为水溶液.据测定,上层物质为乙醛的加合物(C2H4O)n,它的沸点比水的沸点高,分子中无醛基.乙醛在溶液中易被氧化,为从变质的乙醛溶液中提取乙醛(仍得到溶液),可利用如下反应原理:(C2H4O)n$\underset{\stackrel{{H}^{+}}{→}}{\;}$n(C2H4O).
市售乙醛通常为40%左右的乙醛溶液.久置的乙醛溶液会产生分层现象,上层为无色油状液体,下层为水溶液.据测定,上层物质为乙醛的加合物(C2H4O)n,它的沸点比水的沸点高,分子中无醛基.乙醛在溶液中易被氧化,为从变质的乙醛溶液中提取乙醛(仍得到溶液),可利用如下反应原理:(C2H4O)n$\underset{\stackrel{{H}^{+}}{→}}{\;}$n(C2H4O).