题目内容
15.下列有关实验操作、现象和解释或结论都正确的是( )| 选项 | 操作 | 现象 | 解释或结论 |
| A | 用容量瓶配制溶液时,定容后摇匀 | 液面低于刻度线 | 浓度一定偏高 |
| B | 燃着的镁条深入盛CO2的集气瓶中 | 镁条继续燃烧 | 镁有比较强的还原性 |
| C | 分别向酸性KMnO4溶液中加入FeCl2或通入SO2 | 酸性KMnO4溶液颜色均褪去 | Fe2+具有还原性,SO2具有漂白性 |
| D | 过量Fe粉加入稀HNO3中,充分反应后,滴入KSCN溶液 | 溶液呈红色 | 稀HNO3将Fe氧化Fe3+ |
| A. | A | B. | B | C. | C | D. | D |
分析 A.摇匀后部分溶液留在刻度线上方,导致液面低于刻度线,对溶液浓度没有影响;
B.根据氧化还原反应中化合价变化判断氧化性、还原性;
C.酸性高锰酸钾溶液具有强氧化性,能够氧化二氧化硫、亚铁离子;
D.过量Fe粉加入稀HNO3中,充分反应后生成亚铁离子,滴入硫氰化钾后不会变红色.
解答 解:A.用容量瓶配制溶液时,定容后摇匀,摇匀刻度线上方有残留溶液,导致液面低于刻度线,属于正常现象,对溶液浓度没有影响,故A错误;
B.燃着的镁条深入盛CO2的集气瓶中,镁条继续燃烧生成氧化镁和碳,证明金属Mg的还原性较强,故B正确;
C.分别向酸性KMnO4溶液中加入FeCl2或通入SO2,亚铁离子、二氧化硫被酸性高锰酸钾溶液氧化,导致酸性KMnO4溶液颜色均褪去,二氧化硫没有表现漂白性,故C错误;
D.过量Fe粉加入稀HNO3中,充分反应后生成硝酸亚铁,滴入KSCN溶液后溶液没有明显现象,故D错误;
故选B.
点评 本题考查了化学实验方案的设计与评价,题目难度中等,涉及溶液配制、氧化性、还原性强弱比较、铁离子、亚铁离子的检验方法,明确常见元素及其化合物性质为解答关键,试题培养了学生的化学实验能力.

练习册系列答案
相关题目
12.牛肉和菠菜等食物中含有丰富的铁,这里的“铁”应理解为( )
| A. | 单质 | B. | 分子 | C. | 原子 | D. | 元素 |
13.氨气与氧气在有催化剂的条件下进行反应,不会发生的现象是( )
| A. | 产生的气体溶于水中,能使酚酞变红 | |
| B. | 催化剂保持红热 | |
| C. | 可能生成红棕色的气体 | |
| D. | 可能产生白烟 |
20.如图为通过手持技术实时测量冰醋酸稀释过程中电导率和温度的变化曲线,下列关于弱电解质溶液电离过程的说法错误的是( )
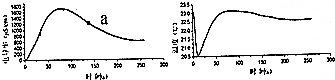

| A. | 冰醋酸稀释过程中,溶液的导电能力先增大后减小 | |
| B. | 左图的曲线也可以表示溶液的pH变化趋势 | |
| C. | 稀释一开始,溶液的温度就下降,可推知电离过程可能是吸热过程 | |
| D. | 可通过微热的方法,使图中a点溶液中的c(CH3COO-)增大 |
7.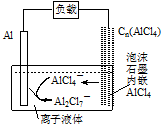 最近中美研究人员发明了一种可快速充放电的铝离子电池,该电池电解质为离子液体{AlCl3/[EMIM]Cl},放电时有关离子转化如图所示.下列说法正确的是( )
最近中美研究人员发明了一种可快速充放电的铝离子电池,该电池电解质为离子液体{AlCl3/[EMIM]Cl},放电时有关离子转化如图所示.下列说法正确的是( )
 最近中美研究人员发明了一种可快速充放电的铝离子电池,该电池电解质为离子液体{AlCl3/[EMIM]Cl},放电时有关离子转化如图所示.下列说法正确的是( )
最近中美研究人员发明了一种可快速充放电的铝离子电池,该电池电解质为离子液体{AlCl3/[EMIM]Cl},放电时有关离子转化如图所示.下列说法正确的是( )| A. | 充电时,阴极发生:4Al2Cl7-+3e-═Al+7AlCl4- | |
| B. | 充电时,泡沫石墨极与外电源的负极相连 | |
| C. | 放电时,负极发生:2AlCl4--e-═Al2Cl7-+Cl- | |
| D. | 放电时,电路中每流过3mol电子,正极减少27g |
4.“保护环境”是我国的基本国策.下列做法不应该提倡的是( )
| A. | 大力推广燃煤发电以满足工业发展的用电需求 | |
| B. | 加强生活污水的除磷处理,遏制水体的富营养化 | |
| C. | 实施化石燃料脱硫硝技术,减少大气污染物的排放 | |
| D. | 用CO2合成聚碳酸酯可降解塑料,实现“碳”的循环利用 |
 某学生为测定未知浓度的硫酸溶液,实验如下:用1.00mL待测硫酸配制100mL稀H2SO4溶液;以0.14mol•L-1的NaOH溶液滴定上述稀H2SO4 25.00mL,滴定终止时消耗NaOH溶液15.00mL.
某学生为测定未知浓度的硫酸溶液,实验如下:用1.00mL待测硫酸配制100mL稀H2SO4溶液;以0.14mol•L-1的NaOH溶液滴定上述稀H2SO4 25.00mL,滴定终止时消耗NaOH溶液15.00mL.