题目内容
某溶液中含有SO32-、Br-、SiO32-、CO32-、Na+,向该溶液中通入过量的Cl2,下列判断正确的是( )
①反应前后,溶液中离子浓度基本保持不变的只有Na+
②有胶状沉淀物质生成
③有气体产生
④溶液颜色发生变化
⑤共发生了2个氧化还原反应.
①反应前后,溶液中离子浓度基本保持不变的只有Na+
②有胶状沉淀物质生成
③有气体产生
④溶液颜色发生变化
⑤共发生了2个氧化还原反应.
| A、①②③④⑤ | B、①②③④ |
| C、①③⑤ | D、②④⑤ |
考点:氯气的化学性质,离子共存问题
专题:卤族元素
分析:某溶液中含有SO32-、SiO32-、Br-、CO32-、Na+,向该溶液中通入过量的Cl2,Cl2与水反应;SO32-可以被氯气氧化为硫酸根离子;SiO32-和氯水中的盐酸反应生成硅酸沉淀;Br-被氯气氧化为溴单质;CO32-和氯水中的盐酸反应生成二氧化碳气体,以此解答该题.
解答:
解:某溶液中含有SO32-、SiO32-、Br-、CO32-、Na+,向该溶液中通入过量的Cl2,SO32-可以被氯气氧化为硫酸根离子;SiO32-和氯水中的盐酸反应生成硅酸沉淀;Br-被氯气氧化为溴单质;CO32-和氯水中的盐酸反应生成二氧化碳气体;
①钠离子不参加反应,反应前后,溶液中离子浓度基本保持不变的有Na+,故①正确;
②SiO32-和氯水中的盐酸反应生成硅酸沉淀,有胶状物质硅酸生成,故②正确;
③CO32-和氯水中的盐酸反应生成二氧化碳气体,故③正确;
④氯气氧化溴离子为溴单质,溶液颜色发生变化有无色变化为橙红色,故④正确;
⑤共发生了氯气与水反应、氧化SO32-、Br-3个氧化还原反应.故⑤错误;
故选B.
①钠离子不参加反应,反应前后,溶液中离子浓度基本保持不变的有Na+,故①正确;
②SiO32-和氯水中的盐酸反应生成硅酸沉淀,有胶状物质硅酸生成,故②正确;
③CO32-和氯水中的盐酸反应生成二氧化碳气体,故③正确;
④氯气氧化溴离子为溴单质,溶液颜色发生变化有无色变化为橙红色,故④正确;
⑤共发生了氯气与水反应、氧化SO32-、Br-3个氧化还原反应.故⑤错误;
故选B.
点评:本题考查了氯水成分和离子反应的判断,主要考查氯气的氧化性、氯水中盐酸的作用,为高频考点,难度不大,注意相关基础知识的积累.

练习册系列答案
相关题目
下列实验不能达到目的是( )
| A、向25mL沸水中滴加5-6滴稀的FeCl3溶液制备氢氧化铁胶体 |
| B、只用少量水就可鉴别Na2CO3和NaHCO3固体 |
| C、用FeSO4、NaOH和盐酸等试剂在空气中可以制备纯净的FeCl3溶液 |
| D、用NaOH溶液和盐酸可除去MgCl2溶液中混有的AlCl3 |
盛浓H2SO4的试剂瓶贴图中最合适的标志是( )
A、 |
B、 |
C、 |
D、 |

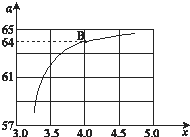 工业生产尿素的原理是以NH3和CO2为原料合成尿素[CO(NH2)2],反应的化学方程式为:2NH3 (g)+CO2 (g?CO(NH2)2 (l)+H2O (l),该反应的平衡常数和温度关系如下:
工业生产尿素的原理是以NH3和CO2为原料合成尿素[CO(NH2)2],反应的化学方程式为:2NH3 (g)+CO2 (g?CO(NH2)2 (l)+H2O (l),该反应的平衡常数和温度关系如下: