题目内容
5.A、B、C、D四种金属分别浸入稀硫酸中,C、D产生气泡缓慢,A、B产生气泡较剧烈.把C、D两金属用导线连接后浸入稀硫酸中,气泡从C金属片析出.把A、B两金属片用导线连接浸入稀硫酸组成原电池时,电流由A→B.根据实验可知,A、B、C、D四种金属的活动性顺序排列是B>A>D>C.分析 根据金属与酸发生反应的条件(在金属的活动性顺序表中排在H前面的金属能与酸发生反应,产生氢气,H后面的金属不能与酸反应)以及金属与盐溶液发生反应的条件(在金属的活动性顺序表中排在前面的金属能把它后面的金属从其盐溶液中置换出来)便可判断金属的活动性强弱.
解答 解:①把A、B、C、D四种金属分别浸入稀硫酸中,A、B产生气泡较剧烈,C、D产生气泡都很慢,所以A、B的活泼性强于C、D;
②把C、D两金属用导线连接后浸入稀硫酸中,气泡从C金属片析出,说明C极是氢离子放电,生成氢气,发生还原反应,所以C是正极,则D的活泼性强于C;
③把A、B两金属片用导线连接浸入稀硫酸组成原电池时,电流由A→B,说明A是正极,B是负极,所以B比A活泼;综上所述金属的活泼性是:B>A>D>C,故答案为:B>A>D>C.
点评 根据金属与酸发生反应的条件、以及金属与盐溶液发生反应的条件,可判断金属的活动性强弱,这一点要求学生要牢牢的掌握.

练习册系列答案
 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案
相关题目
15.在由水电离产生的H+浓度为1×10-13mol•L-1的溶液中,一定能大量共存的离子组是( )
| A. | K+、Cl-、NO3-、S2- | B. | Na+、Cl-、NO3-、SO42- | ||
| C. | K+、Fe2+、I-、SO42- | D. | Na+、Ca2+、Cl-、HCO3- |
20.2011年“国际化学年”的主题是“化学,我们的生活,我们的未来”.下列行为中不符合这一主题的是( )
| A. | 用CO2合成可降解塑料,实现碳的循环利用 | |
| B. | 提倡使用太阳能、潮汐能、风能等清洁能源,减少化石燃料的使用 | |
| C. | 提高煤炭和石油的产量,以满足工业生产的快速发展 | |
| D. | 实现资源的“3R”利用,即减少资源消耗(Reduce)、增加资源的重复使用(Reuse)、提高资源的循环利用(Recycle) |
10.将标准状况下的H2S气体通入100mL 5mol?L-1的CuSO4溶液中,再向混合溶液中滴加2mol?L-1NaOH溶液,当溶液的pH=7时,滴入的NaOH溶液体积为( )
| A. | 500mL | B. | 250mL | C. | 200mL | D. | 100mL |
17.已知可逆反应aA+bB?cC中,物质的含量A%和C%随温度的变化曲线如图所示,下列说法正确的是( )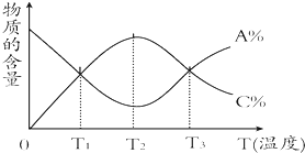

| A. | 该反应在T1、T3温度时达到化学平衡 | |
| B. | 该反应在T2温度时未达到化学平衡 | |
| C. | 升高温度,平衡会向正反应方向移动 | |
| D. | 该反应的正反应是放热反应 |
14.将下列各组物质按单质、氧化物、酸、碱、盐分类顺序排列,其中正确的是( )
| A. | 液态氧、干冰、硫酸、烧碱、氯化钠 | B. | 碘酒、冰、盐酸、烧碱、食盐 | ||
| C. | 氢气、二氧化硫、硝酸、纯碱、硝酸钾 | D. | 铜、硫酸钠、醋酸、石灰水、氯化铜 |
15.在一定条件下,将PCl3(g)和Cl2(g)充入体积不变的2L密闭容器中发生下述反应:PCl3(g)+Cl2(g)?PCl5(g);5min末达到平衡,有关数据如表.
下列判断不正确的是( )
| PCl3(g) | Cl2(g) | PCl5(g) | |
| 初始浓度(mol•L-1) | 2.0 | 1.0 | 0 |
| 平衡浓度(mol•L-1) | c1 | c2 | 0.4 |
| A. | 若升高温度,反应的平衡常数减小,则正反应为吸热反应 | |
| B. | 反应5 min内,v(PCl3)=0.08 mol•L-1•min-1 | |
| C. | 当容器中为1.2 mol Cl2时,可逆反应达到平衡状态 | |
| D. | 平衡后移走2.0 mol PCl3和1.0 mol Cl2,在相同条件下再达平衡时,c(PCl5)<0.2 mol/L |
 ;.
;. 水不仅是包括人类在内所有生命生存的重要资源,也是化学反应中的重要物质:
水不仅是包括人类在内所有生命生存的重要资源,也是化学反应中的重要物质: