题目内容
12.科学家发现用二氧化钛(TiO2)作催化剂可以使水在光照条件下分解制得廉价的氢气,这使氢能源的研究和应用更向前迈进了一步.下列说法正确的是( )| A. | 使用二氧化钛作催化剂使水快速分解的同时放出大量热 | |
| B. | 催化剂的作用是改变反应所需要达到的活化能来增大反应的速率 | |
| C. | 该反应的原理是:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2+O2 | |
| D. | 每产生氢气44.8L,转移电子数目为4NA |
分析 A、水分解是吸热反应;
B、使用催化剂加快化学反应速率;
C、该反应的原理是:2H2O$\frac{\underline{\;TiO_{2}\;}}{光照}$ 2H2↑+O2↑;
D、状况不知,无法由体积求物质的量.
解答 解:A、催化剂的使用未改变反应的热效应,而水分解是吸热反应,故A错误;
B、使用催化剂加快化学反应速率,所以改变反应所需要时间,故B正确;
C、该反应的原理是:2H2O$\frac{\underline{\;TiO_{2}\;}}{光照}$ 2H2↑+O2↑,故C错误;
D、状况不知,无法由体积求物质的量,所以转移电子数目不知,故D错误;
故选B.
点评 本题考查催化剂的含义和气体摩尔体积的应用,以及方程式的书写,综合性强,但比较容易.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
20.在碱性溶液中能大量共存且溶液为无色透明的离子组是( )
| A. | K+、MnO4-、Na+、Cl- | B. | Fe3+、Na+、Cl-、SO42- | ||
| C. | NH4+、Na+、NO3-、CO32- | D. | Na+、K+、SiO32-、NO3- |
17.下列叙述正确的是( )
| A. | 铝制品的耐腐蚀性强,说明铝的化学性质不活泼 | |
| B. | 铁板上镀锡属于电化学防护 | |
| C. | 生铁中含有碳,抗腐蚀能力比纯铁强 | |
| D. | 将海水中的钢铁闸门与电源的负极相连,可防止闸门被腐蚀 |
4.在一密闭容器中,反应aA(g)?bB(g)达到平衡后,保持温度不变,将容器体积减小为原来体积的1/2,达到新的平衡时,B的浓度是原来的1.5倍,下列说法正确的是( )
| A. | 平衡向正反应方向移动了 | B. | 物质A的转化率增大 | ||
| C. | 物质B的质量分数减小了 | D. | a>b |
17.下列说法错误的是( )
| A. | 硅胶可用作食品干操剂 | |
| B. | P2O5不可用作食品干操剂 | |
| C. | 六水氯化钙可用作食品干燥剂 | |
| D. | 加工后具有吸水性的植物纤维可用作食品干燥剂 |
 Cl02气体是一种常用的消毒剂,我国从2000年起逐步用Cl02代替氯气对饮用水进行消毒.但二氧化氯是一种极易爆炸的强氧化性气体,易溶于水、不稳定、呈黄绿色,在生产和使用时必须尽量用稀有气体进行稀释,同时需要避免光照、震动或加热.
Cl02气体是一种常用的消毒剂,我国从2000年起逐步用Cl02代替氯气对饮用水进行消毒.但二氧化氯是一种极易爆炸的强氧化性气体,易溶于水、不稳定、呈黄绿色,在生产和使用时必须尽量用稀有气体进行稀释,同时需要避免光照、震动或加热.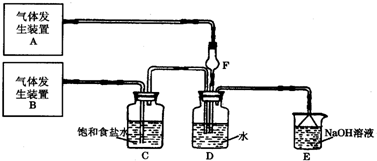
 化学是一门以实验为基础的学科,化学所取得的丰硕成果,是与实验的重要作用分不开的.结合实验装置图回答问题:
化学是一门以实验为基础的学科,化学所取得的丰硕成果,是与实验的重要作用分不开的.结合实验装置图回答问题: