题目内容
6.下列有关热化学方程式的叙述正确的是( )| A. | 已知2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ•mol-1,则氢气的标准燃烧热为-483.6kJ/mol | |
| B. | △H的数值与化学反应方程式的化学计量系数无关 | |
| C. | 含20.0g NaOH的稀溶液与稀硫酸完全中和,放出28.7kJ的热量,则该反应的热化学方程式为:NaOH(aq)+$\frac{1}{2}$H2SO4(aq)═$\frac{1}{2}$Na2SO4(aq)+H2O(l)△H=-57.4 kJ•mol-1 | |
| D. | 己知C(s)+O2(g)═CO2(g)△H1;C(g)+O2(g)═CO2(g)△H2,则△H1<△H2 |
分析 A、燃烧热是1mol可燃物完全燃烧生成稳定氧化物放出的热量分析;
B、△H的数值与化学反应方程式的化学计量系数成正比;
C、依据酸碱中和热的概念分析,中和热是强酸强碱的稀溶液完全反应生成1mol水放出的热量;
D、固体到气体要吸热,反应热大小比较包括正负.
解答 解:A、燃烧热是1mol可燃物完全燃烧生成稳定氧化物放出的热量分析,选项中水是气体不是液态氧化物,故燃烧热大于241.8kJ/mol,故A错误;
B、△H的数值与化学反应方程式的化学计量系数成正比,故B错误;
C、依据酸碱中和热的概念分析,中和热是强酸强碱的稀溶液完全反应生成1mol水放出的热量,含20.0g NaOH物质的量为0.5mol的稀溶液与稀硫酸完全中和,放出28.7kJ的热量,则表示该反应中和热的热化学方程式为:NaOH(aq)+$\frac{1}{2}$H2SO4(aq)═$\frac{1}{2}$Na2SO4(aq)+H2O(l)△H=-57.4kJ/mol,故C正确;
D、固体到气体要吸热,反应热大小比较包括正负,所以气体碳放出的热量多,而反应热大小比较包括正负,所以△H1>△H2,故D错误;
故选C.
点评 本题考查了燃烧热、中和热概念的理解应用,反应热大小比较,注意焓变为负值,题目难度中等.

练习册系列答案
相关题目
11.下列关于浓硫酸的叙述正确的是( )
| A. | 浓硫酸具有吸水性,因而能使蔗糖炭化 | |
| B. | 蓝色的胆矾晶体中加入浓硫酸,晶体会转化为白色固体 | |
| C. | 浓硫酸是一种干燥剂,能够干燥氨气、氢气等气体 | |
| D. | 常温下,浓硫酸不与铁、铝反应,所以可以用铁、铝制容器盛装浓硫酸 |
18.下列有关硅及其化合物的说法中正确的是( )
| A. | 陶瓷、玻璃、水泥容器都能贮存氢氟酸 | |
| B. | 硅酸钠属于盐,不属于碱,所以硅酸钠可以保存在磨口玻璃塞的试剂瓶中 | |
| C. | 用SiO2制取硅酸,应先使二氧化硅与氢氧化钠溶液反应,然后再通入CO2 | |
| D. | 由Na2CO3+SiO2 $\frac{\underline{\;高温\;}}{\;}$CO2+Na2SiO3可知硅酸的酸性大于碳酸 |
15.下表是不同温度下水的离子积数据:
试回答下列问题:
(1)若25<t1<t2,则t1℃时纯水中c (H+)=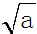 mol•L-1.
mol•L-1.
(2)25℃下,某Na2SO4溶液中c(SO42-)=5×10-4 mol•L-1,取该溶液1mL,加水稀释至100mL,则稀释后溶液中c (Na+):c (OH-)=100:1
(3)t2℃下,将pH=10的苛性钠溶液V1 L与pH=1的稀硫酸V2 L混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的pH=2,则V1:V2=9:2.此溶液中各种离子的浓度由大到小的排列顺序是c(H+)>c(SO42-)>c(Na+)>c(OH-).
| 温度/℃ | 25 | t1 | t2 |
| 水的离子积常数 | 1×10-14 | α | 1×10-12 |
(1)若25<t1<t2,则t1℃时纯水中c (H+)=
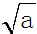 mol•L-1.
mol•L-1.(2)25℃下,某Na2SO4溶液中c(SO42-)=5×10-4 mol•L-1,取该溶液1mL,加水稀释至100mL,则稀释后溶液中c (Na+):c (OH-)=100:1
(3)t2℃下,将pH=10的苛性钠溶液V1 L与pH=1的稀硫酸V2 L混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的pH=2,则V1:V2=9:2.此溶液中各种离子的浓度由大到小的排列顺序是c(H+)>c(SO42-)>c(Na+)>c(OH-).
1.在溶液中能够大量共存的离子组是( )
| A. | Ca+、Cl-、CO32-、Na+ | B. | Cl-、CO32-、Na+、H+ | ||
| C. | H+、Ba2+、OH-、NO3- | D. | Mg2+、Na+、Cl-、SO42- |