题目内容
将A g粗盐样品溶于水,所得溶液中含有Ca2+、Mg2+等杂质离子,现设计实验,采用常见的试剂,精制食盐溶液.回答下列问题:
(1)为了除去粗盐中的CaCl2、MgCl2、Na2SO4及泥沙.可将粗盐溶于水,此时可以观察到的实验现象为 .溶解时玻璃棒的作用为 .
(2)在步骤(1)之后进行下列五项操作:①过滤;②加过量NaOH溶液;③加适量盐酸;④加过量Na2CO3溶液;⑤加过量BaCl2溶液.正确的操作顺序是 (填代号).
A.⑤④②①③B.④①②⑤③C.②⑤④①③D.⑤②④①③
(3)在进行步骤(2)的实验中,检验SO42-沉淀是否完全的方法是
(4)检验提纯后的食盐溶液中是否含有SO42-的方法是:取少量溶液置于试管中,向溶液中加入足量的 ,然后加入几滴 溶液,若产生白色沉淀说明有SO42-;若不产生白色沉淀说明无SO42-.
(5)在蒸发NaCl溶液时,一般的有以下步骤:①放置酒精灯;②固定铁圈位置;③放上蒸发皿;④加热搅拌;⑤停止加热.正确的操作顺序是 .
(6)实验完毕得到Bg固体,则原样品中Na+质量为 .
A.<23A/58.5 B.>23A/58.5 C.<23B/58.5 D.>23B/58.5.
(1)为了除去粗盐中的CaCl2、MgCl2、Na2SO4及泥沙.可将粗盐溶于水,此时可以观察到的实验现象为
(2)在步骤(1)之后进行下列五项操作:①过滤;②加过量NaOH溶液;③加适量盐酸;④加过量Na2CO3溶液;⑤加过量BaCl2溶液.正确的操作顺序是
A.⑤④②①③B.④①②⑤③C.②⑤④①③D.⑤②④①③
(3)在进行步骤(2)的实验中,检验SO42-沉淀是否完全的方法是
(4)检验提纯后的食盐溶液中是否含有SO42-的方法是:取少量溶液置于试管中,向溶液中加入足量的
(5)在蒸发NaCl溶液时,一般的有以下步骤:①放置酒精灯;②固定铁圈位置;③放上蒸发皿;④加热搅拌;⑤停止加热.正确的操作顺序是
(6)实验完毕得到Bg固体,则原样品中Na+质量为
A.<23A/58.5 B.>23A/58.5 C.<23B/58.5 D.>23B/58.5.
考点:粗盐提纯
专题:实验题
分析:(1)根据粗盐中含有不溶性泥沙来分析现象,在固体溶解的过程中,玻璃棒的作用是搅拌;
(2)在粗盐的提纯过程中,氯化钡的加入必须在碳酸钠之前,过滤之后才能加盐酸,据此得出操作顺序;
(3)检验SO42-是否沉淀完全可以采用反滴法;
(4)根据SO42-的检验方法来分析;
(5)组装仪器的一般顺序是采用先下后上,先左后右的原则,利用本规则即可解答.
(6)根据最后所得的Bg氯化钠中的Na+的来源来计算.
(2)在粗盐的提纯过程中,氯化钡的加入必须在碳酸钠之前,过滤之后才能加盐酸,据此得出操作顺序;
(3)检验SO42-是否沉淀完全可以采用反滴法;
(4)根据SO42-的检验方法来分析;
(5)组装仪器的一般顺序是采用先下后上,先左后右的原则,利用本规则即可解答.
(6)根据最后所得的Bg氯化钠中的Na+的来源来计算.
解答:
解:(1)粗盐中含有不溶性泥沙,故将粗盐溶于水,此时可以观察到的实验现象为得到浑浊的溶液,在固体溶解的过程中,玻璃棒的作用是搅拌,加速溶解,
故答案为:得到溶解的液体;搅拌,加速溶解;
(2)在粗盐的提纯过程中,氯化钡的加入必须在碳酸钠之前,过滤之后才能加盐酸,据此得出操作顺序为⑤④②①③或②⑤④①③或⑤②④①③,故选ACD;
(3)检验SO42-是否沉淀完全可以采用反滴法,故可以采用取上层清液少许于试管中,滴加BaCl2溶液,如无沉淀生成,则表明SO42-已沉淀完全;如有沉淀生成,则表明SO42-未沉淀完全.故答案为:取上层清液少许于试管中,滴加BaCl2溶液,如无沉淀生成,则表明SO42-已沉淀完全;如有沉淀生成,则表明SO42-未沉淀完全;
(4)SO42-的检验主要用氯化钡,要先加盐酸排除CO32-、Ag+等干扰离子,故检验方法为:先加稀盐酸,然后滴加氯化钡溶液,如果有沉淀生成,则说明溶液中有SO42-,
故答案为:稀HCl;BaCl2;
(5)组装仪器时要从下向上组装,酒精灯在铁圈和蒸发皿的下方,所以要先放酒精灯;然后再固定铁圈,放置蒸发皿;然后再点燃酒精灯加热,并搅拌,当有较多晶体析出时,停止加热,借余热蒸干.正确的操作顺序为①②③④⑤,故答案为:①②③④⑤;
(6)在A g粗盐中,除了氯化钠还含有其他杂质,故原样品中Na+的质量m<23A/58.5;实验完毕得到BgNaCl中,一部分Na+自于粗盐样品,还有一部分来自于加入的NaOH和Na2CO3,故原样品中Na+质量m<23B/58.5g,故选AC.
故答案为:得到溶解的液体;搅拌,加速溶解;
(2)在粗盐的提纯过程中,氯化钡的加入必须在碳酸钠之前,过滤之后才能加盐酸,据此得出操作顺序为⑤④②①③或②⑤④①③或⑤②④①③,故选ACD;
(3)检验SO42-是否沉淀完全可以采用反滴法,故可以采用取上层清液少许于试管中,滴加BaCl2溶液,如无沉淀生成,则表明SO42-已沉淀完全;如有沉淀生成,则表明SO42-未沉淀完全.故答案为:取上层清液少许于试管中,滴加BaCl2溶液,如无沉淀生成,则表明SO42-已沉淀完全;如有沉淀生成,则表明SO42-未沉淀完全;
(4)SO42-的检验主要用氯化钡,要先加盐酸排除CO32-、Ag+等干扰离子,故检验方法为:先加稀盐酸,然后滴加氯化钡溶液,如果有沉淀生成,则说明溶液中有SO42-,
故答案为:稀HCl;BaCl2;
(5)组装仪器时要从下向上组装,酒精灯在铁圈和蒸发皿的下方,所以要先放酒精灯;然后再固定铁圈,放置蒸发皿;然后再点燃酒精灯加热,并搅拌,当有较多晶体析出时,停止加热,借余热蒸干.正确的操作顺序为①②③④⑤,故答案为:①②③④⑤;
(6)在A g粗盐中,除了氯化钠还含有其他杂质,故原样品中Na+的质量m<23A/58.5;实验完毕得到BgNaCl中,一部分Na+自于粗盐样品,还有一部分来自于加入的NaOH和Na2CO3,故原样品中Na+质量m<23B/58.5g,故选AC.
点评:本题考查在粗盐提纯的过程中所选用除杂和净化的方法,难度不大,除去杂质不要引入新的杂质,对于实验过程中过量的试剂都要除去.

练习册系列答案
相关题目
为迎接北京奥运,北京曾采用机动车按照单双号行驶的方案,该方案既保障了交通秩序,又大大减少了空气污染.汽车尾气中所含污染物除碳氢化合物、可吸入颗粒物、一氧化碳外,还主要含有( )
| A、氮气 | B、硫化氢 |
| C、二氧化硫 | D、氮的氧化物 |
 可逆反应在一定条件下达到平衡后,速率差值[即v(正)-v(逆)]与压强的变化曲线如图所示,其中与曲线①相符的反应为( )
可逆反应在一定条件下达到平衡后,速率差值[即v(正)-v(逆)]与压强的变化曲线如图所示,其中与曲线①相符的反应为( )| A、2SO3(g)?2SO2(g)+02(g) |
| B、H2(g)+I2(g)?2HI(g) |
| C、C(s)+H2O(g)?C0(g)+H2(g) |
| D、N2(g)+3H2(g)?2NH3(g) |
0.4mol CuSO4和0.4mol NaCl溶于水,配成1L溶液,用惰性电极进行电解,当一个电极得到0.3mol Cu时,另一个电极上生成的气体在标准状况下的体积是( )
| A、5.6L |
| B、6.72L |
| C、1.344L |
| D、11.2L |
下列反应,①符合图象描述特点,②对其进行分析,结论是正确的.则合理选项为( )
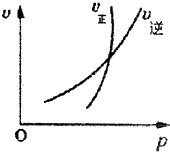

| A、2NO2(g)?N2O4(g);平衡后增大压强,气体颜色先变深后变浅 |
| B、N2(g)+3H2(g)?2NH3(g);将氨气液化分离后,有利于加快正反应速率 |
| C、4NH3(g)+5O2(g)?4NO(g)+6H2O(g);加大氧气浓度,能提高氨气平衡转化率 |
| D、2HI(g)?H2(g)+I2(g);平衡后又充入一定量HI,再次平衡时HI的转化率不变 |
为鉴别K2CO3和NaHCO3两种白色固体,有四名同学分别设计了下列四种不同的方法,其中不可行的是( )
| A、分别滴加0.1 mol?L-1的盐酸,看气泡产生的快慢 |
| B、分别取样在试管中加热,将可能产生的气体通入澄清石灰水,观察有无白色沉淀生成 |
| C、分别取样配成溶液,滴加Ba(OH)2溶液,观察有无白色沉淀 |
| D、分别配成溶液,做焰色反应实验,观察火焰的颜色 |
初中化学教材中“家庭小实验”是利用家庭日常生活用品进行化学学习和探究的活动.食盐、食醋、纯碱等均为家庭厨房中常用的物质,利用这些物质你能完成的实验是( )
①检验自来水中是否含氯离子
②鉴别食盐和纯碱
③检验鸡蛋壳能否溶于酸
④除去热水瓶中的水垢.
①检验自来水中是否含氯离子
②鉴别食盐和纯碱
③检验鸡蛋壳能否溶于酸
④除去热水瓶中的水垢.
| A、①②③④ | B、①③ |
| C、②④ | D、②③④ |
一定条件下,在2L的密闭容器中发生可逆反应:Fe(s)+CO(g)?Fe(s)+CO2(g),已知该反应的平衡常数(K)与温度(T)的关系如图甲,图乙是T1温度下该反应的c-t关系图象.则下列说法正确的是( )


| A、保持恒容恒温条件,向密闭容器中充入氦气,化学反应速率将变快 |
| B、若容器的容积不变,降低温度,c(CO2)/c(CO)减小 |
| C、保持恒容恒温(T1)条件,8min达化学平衡状态时,v(CO)=0.0625mol/(L?s) |
| D、保持恒容恒温(T1)条件,8min后再加入足量FeO粉末并充入1.5mol的CO气体,重新达到平衡时,CO的转化率为33.3% |