题目内容
0.4mol CuSO4和0.4mol NaCl溶于水,配成1L溶液,用惰性电极进行电解,当一个电极得到0.3mol Cu时,另一个电极上生成的气体在标准状况下的体积是( )
| A、5.6L |
| B、6.72L |
| C、1.344L |
| D、11.2L |
考点:电解原理
专题:电化学专题
分析:电解硫酸铜和氯化钠溶液时,阳极上氯离子先放电,然后氢氧根离子放电,阴极上铜离子放电,后氢离子放电,当阴极上析出析出铜的物质的量为0.3mol<0.4mol,根据转移电子守恒计算阳极上生成气体体积.
解答:
解:电解硫酸铜和氯化钠溶液时,阳极上氯离子先放电,然后氢氧根离子放电,阴极上铜离子放电,后氢离子放电,当阴极上析出析出铜的物质的量为0.3mol,阴极上转移电子的物质的量=0.3mol×2=0.6mol,
根据原子守恒知,溶液中n(Cl-)=0.4mol,氯离子完全放电时转移电子的物质的量=0.4mol×1=0.4mol,
所以阳极上生成的气体是氯气和氧气,生成氯气的体积=
×22.4L/mol=4.48L,根据电极反应,4OH--4e-=2H2O+O2↑,转移0.2mol电子,生成氧气的物质的量是0.05mol,即1.12L,所以另一个电极上生成的气体在标准状况下的体积是体积是4.48L+1.12L=5.6L.
故选A.
根据原子守恒知,溶液中n(Cl-)=0.4mol,氯离子完全放电时转移电子的物质的量=0.4mol×1=0.4mol,
所以阳极上生成的气体是氯气和氧气,生成氯气的体积=
| 0.4mol |
| 2 |
故选A.
点评:本题考查了电解原理,明确阴阳极上离子放电顺序是解本题关键,注意要首先根据转移电子相等判断阳极上生成气体成分,再计算其体积,为易错点.

练习册系列答案
 一线名师权威作业本系列答案
一线名师权威作业本系列答案
相关题目
用惰性电极实现电解,下列说法中正确的是( )
| A、电解硫酸铜溶液,加入CuO可使电解后的溶液恢复到原状态 |
| B、电解硝酸银溶液,在阴极上和阳极上析出产物的物质的量之比为1:2 |
| C、电解氯化钾溶液,要消耗H+,故溶液pH减小 |
| D、电解稀硫酸溶液,实质上是电解水,故溶液pH不变 |
哥本哈根世界气候大会上,商讨了《京都议定书》一期承诺到期后的后续方案,即2012年至2020年的全球减排协议.大会倡导“节能减排”和“低碳经济”.下列做法不符合这一理念的是( )
| A、推广利用CO2与环氧丙烷和琥珀酸酐的三元共聚物的生物降解材料 |
| B、使用填埋法处理未经分类的生活垃圾 |
| C、推广煤的干馏、气化、液化技术,提供清洁、高效燃料和基础化工原料 |
| D、发展水电,开发新能源,如核能、太阳能、风能等,减少对化石能源的依赖 |
向一体积不变的密闭容器中加入2mol A、0.6mol C和一定量的B三种气体.一定条件下发生反应,各物质浓度随时间变化如图一所示.图二为 t2时刻后改变反应条件,平衡体系中反应速率随时间变化的情况,且四个阶段都各改变一种不同的条件.已知 t3~t4阶段为使用催化剂;图一中 t0~t1阶段c(B)未画出.下列说法不正确的是( )
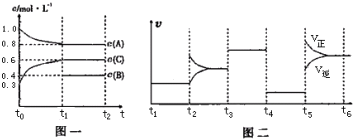

| A、此温度下该反应的化学方程式2A(g)+B(g)?2C(g) | ||||
| B、t4~t5阶段改变的条件为减小压强 | ||||
| C、B 的起始物质的量为1.0mol | ||||
D、在相同条件下,若起始时容器中加入amol A、bmol B 和cmol C,要达到 t1时刻同样的平衡,a、b、c 要满足的条件为a+
|
下列各项实验操作正确的是( )
| A、使C2H5Br和NaOH溶液混合后水解,取上层清液,滴加AgNO3溶液检验溴元素 |
| B、为增强高锰酸钾溶液的氧化性,可用盐酸将高锰酸钾溶液酸化 |
| C、将苯与溴水混合后,再加铁粉,即可制得溴苯 |
| D、在测定盐酸和氢氧化钠溶液反应的中和热时,氢氧化钠溶液应过量 |
关于溴乙烷与NaOH的乙醇溶液共热时反应的现象和产物检验等,说法正确的是( )
| A、实验中可观察到有气体生成 |
| B、往反应后的溶液中直接加入AgNO3溶液可检验是否有Br-生成 |
| C、逸出的气体可直接通入到酸性高锰酸钾溶液中检验是否有乙烯生成 |
| D、生成的产物只有一种 |
下列说法不正确的是( )
| A、油脂是高级脂肪酸的甘油酯 |
| B、油脂与氢气发生加成反应,可以得到硬化油 |
| C、油脂在酸性条件或碱性条件下,可以发生皂化反应 |
| D、日常使用的花生油、豆油、动物油都是油脂,它们可以溶解一些脂溶性维生素 |
 为除去粗盐中的Ca2+、Mg2+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
为除去粗盐中的Ca2+、Mg2+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):