题目内容
已知某些金属氧化物跟熔融烧碱反应可生成盐.根据下图所示化学反应回答下列问题.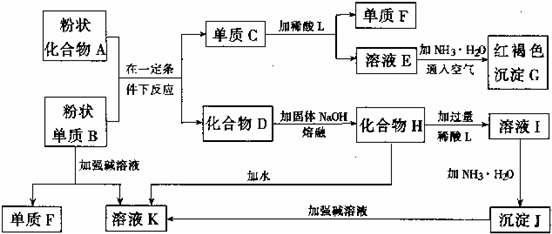
(1)单质F的化学式为 .
(2)写出下列反应的离子方程式:C+L-→F+E H+L(过量)-→I
(3)C+L-→E+F,若L改用浓酸,则不能选用的浓酸是(写分子式) .

(1)单质F的化学式为
(2)写出下列反应的离子方程式:C+L-→F+E
(3)C+L-→E+F,若L改用浓酸,则不能选用的浓酸是(写分子式)
考点:无机物的推断
专题:推断题
分析:G是红棕色沉淀,则G是Fe(OH)3,E和氨水、空气反应生成氢氧化铁,则E中含有亚铁离子,则单质C为Fe,铁和酸反应生成亚铁盐和氢气,所以F是H2;
粉末状单质B能和强碱溶液反应生成氢气和溶液K,两种固体在一定条件下反应生成铁,且B为单质,说明二者发生铝热反应,则B是Al,D为Al2O3,A为铁的氧化物,K为偏铝酸盐,氧化铝和氢氧化钠溶液反应生成偏铝酸钠和水,所以H为NaAlO2,H溶于水生成偏铝酸钠溶液,所以K为NaAlO2,偏铝酸钠和过量酸反应生成铝盐,铝盐和氨水反应生成Al(OH)3,所以J是Al(OH)3,再结合题目解答.
粉末状单质B能和强碱溶液反应生成氢气和溶液K,两种固体在一定条件下反应生成铁,且B为单质,说明二者发生铝热反应,则B是Al,D为Al2O3,A为铁的氧化物,K为偏铝酸盐,氧化铝和氢氧化钠溶液反应生成偏铝酸钠和水,所以H为NaAlO2,H溶于水生成偏铝酸钠溶液,所以K为NaAlO2,偏铝酸钠和过量酸反应生成铝盐,铝盐和氨水反应生成Al(OH)3,所以J是Al(OH)3,再结合题目解答.
解答:
解:G是红棕色沉淀,则G是Fe(OH)3,E和氨水、空气反应生成氢氧化铁,则E中含有亚铁离子,则单质C为Fe,铁和酸反应生成亚铁盐和氢气,所以F是H2;
粉末状单质B能和强碱溶液反应生成氢气和溶液K,两种固体在一定条件下反应生成铁,且B为单质,说明二者发生铝热反应,则B是Al,D为Al2O3,A为铁的氧化物,K为偏铝酸盐,氧化铝和氢氧化钠溶液反应生成偏铝酸钠和水,所以H为NaAlO2,H溶于水生成偏铝酸钠溶液,所以K为NaAlO2,偏铝酸钠和过量酸反应生成铝盐,铝盐和氨水反应生成Al(OH)3,所以J是Al(OH)3,
(1)通过以上分析知,F为H2,故答案为:H2;
(2)铁和酸反应生成亚铁离子和氢气,离子方程式为Fe+2H+=Fe2++H2↑,偏铝酸钠和过量酸反应生成铝盐和水,离子方程式为AlO2-+4H+=Al3++2H2O,
故答案为:Fe+2H+=Fe2++H2↑;AlO2-+4H+=Al3++2H2O;
(3)常温下,浓硫酸、浓硝酸和铁发生钝化现象,所以不能选浓硫酸、浓硝酸,故答案为:H2SO4或HNO3.
粉末状单质B能和强碱溶液反应生成氢气和溶液K,两种固体在一定条件下反应生成铁,且B为单质,说明二者发生铝热反应,则B是Al,D为Al2O3,A为铁的氧化物,K为偏铝酸盐,氧化铝和氢氧化钠溶液反应生成偏铝酸钠和水,所以H为NaAlO2,H溶于水生成偏铝酸钠溶液,所以K为NaAlO2,偏铝酸钠和过量酸反应生成铝盐,铝盐和氨水反应生成Al(OH)3,所以J是Al(OH)3,
(1)通过以上分析知,F为H2,故答案为:H2;
(2)铁和酸反应生成亚铁离子和氢气,离子方程式为Fe+2H+=Fe2++H2↑,偏铝酸钠和过量酸反应生成铝盐和水,离子方程式为AlO2-+4H+=Al3++2H2O,
故答案为:Fe+2H+=Fe2++H2↑;AlO2-+4H+=Al3++2H2O;
(3)常温下,浓硫酸、浓硝酸和铁发生钝化现象,所以不能选浓硫酸、浓硝酸,故答案为:H2SO4或HNO3.
点评:本题考查无机物推断,正确找出题中突破口是解本题关键,再结合物质之间转化关系采用正逆结合方法进行推断,注意稀硝酸和铁反应不生成气体单质,为易错点.

练习册系列答案
 一线名师权威作业本系列答案
一线名师权威作业本系列答案
相关题目
放射性同位素钬16667Ho 的原子核内的中子数是( )
| A、99 | B、67 | C、166 | D、32 |
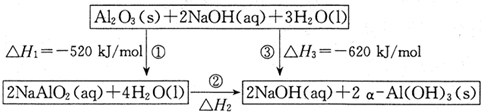
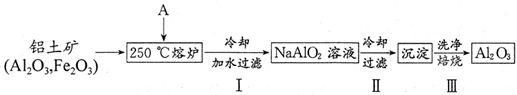
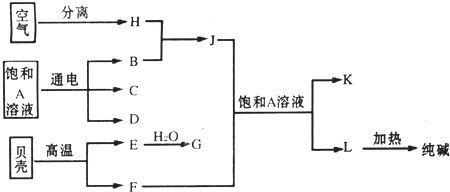

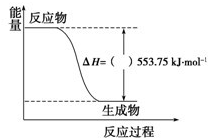 (1)许多运动会使用的火炬内熊熊大火来源于丙烷的燃烧,丙烷是一种优良的燃料.试回答下列问题:
(1)许多运动会使用的火炬内熊熊大火来源于丙烷的燃烧,丙烷是一种优良的燃料.试回答下列问题: