题目内容
20.NA为阿伏加德罗常数的值,下列说法正确的是( )| A. | 2.4g镁在二氧化碳中燃烧所转移的电子总数为0.2NA | |
| B. | 7.1g Cl2与足量NaOH(aq)反应时转移的电子总数为0.2 NA | |
| C. | 1 L1 mol/L的Na2CO3(aq)中CO32-与HCO3-的离子数之和为NA | |
| D. | 1 mol NaHSO4晶体中离子总数为3NA |
分析 A.镁为+2价金属,2.4g镁的物质的量为0.1mol,完全反应失去0.2mol电子;
B.氯气与氢氧化钠溶液的反应中,氯气既是氧化剂也是还原剂,7.1g氯气的物质的量为0.2mol,与氢氧化钠溶液完全反应转移了0.1mol电子;
C.根据碳酸钠溶液中的物料守恒判断;
D.硫酸氢钠晶体中含有钠离子和硫酸氢根离子.
解答 解:A.2.4g镁的物质的量为:$\frac{2.4g}{24g/mol}$=0.1mol,0.1mol镁与二氧化碳完全反应生成0.1mol氧化镁,转移了0.2mol电子,转移的电子总数为0.2NA,故A正确;
B.7.1g氯气的物质的量为:$\frac{7.1g}{71g/mol}$=0.1mol,0.1mol氯气与足量氢氧化钠溶液反应生成0.1mol氯化钠和0.1mol次氯酸钠,转移了0.1mol电子,转移的电子总数为0.1NA,故B错误;
C.1 L1 mol/L的Na2CO3(aq)中含有溶质碳酸钠1mol,根据物料守恒可知,CO32-、HCO3-和H2CO3的物质的量之和为1mol,则CO32-与HCO3-的离子数之和小于NA,故C错误;
D.1molmol NaHSO4晶体中含有1mol钠离子和1mol硫酸氢根离子,总共含有2mol离子,含有的离子总数为2NA,故D错误;
故选A.
点评 本题考查了阿伏伽德罗常数的综合应用,题目难度中等,注意掌握物质的量与阿伏伽德罗常数、摩尔质量等物理量在的转化关系,D为易错点,注意硫酸氢钠晶体中含有的离子为钠离子和硫酸氢根离子.

练习册系列答案
相关题目
10.下列说法中正确的是( )
| A. | 乙烯中碳碳双键的键能是乙烷中碳碳单键的键能的2倍 | |
| B. | 对羟基苯甲醛的沸点比邻羟基苯甲醛高 | |
| C. | 顺-2-丁烯和反-2-丁烯的加氢产物不同 | |
| D. | NH4+中4个N-H键的键能不相同 |
11.2005年6月,国内某知名媒体报道,国内啤酒生产企业中95%以上在生产过程中都填加了甲醛作为添加剂,在啤酒行业内引起极大反响.下列关于甲醛的说法中正确的是( )
| A. | 甲醛分子组成中仅有C、H两种元素 | |
| B. | 甲醛是一种无色无味的气体,对人体无危害,所以,可以放心饮用啤酒 | |
| C. | 甲醛的化学性质很稳定,很难与强酸、强碱、强氧化剂反应 | |
| D. | 甲醛既可以被氧化生成甲酸、也可以还原生成甲醇 |
8.用铂(惰性)电极进行电解,下列说法中正确的是( )
| A. | 电解稀硫酸溶液,实质上是电解水,故溶液pH不变 | |
| B. | 电解稀氢氧化钠溶液,要消耗OH-,故溶液pH减小 | |
| C. | 电解硫酸钠溶液,在阴极上和阳极上析出产物的物质的量之比为1:2 | |
| D. | 电解氯化铜溶液,在阴极上和阳极上析出产物的物质的量之比为1:1 |
5.下列叙述错误的是( )
| A. | 苯、乙烯都既能发生加成反应,也能发生氧化反应 | |
| B. | 塑料、橡胶和合成纤维都属于有机高分子化合物 | |
| C. | 糖类、脂肪和蛋白质在一定条件下都能发生水解反应 | |
| D. | 分子式为C5H12的有机物有三种,它们属于同分异构体 |
12.关于下列各图的叙述中,正确的是( )
| A. | 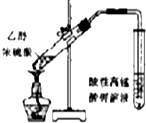 如图装置检验加热时产生的乙烯 | |
| B. | 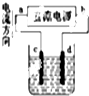 如图装置精炼铜,则d极为粗铜,c极为纯铜,电解质溶液为CuSO4溶液. | |
| C. | 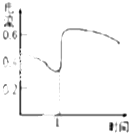 如图表示Zn-Cu原电池反应过程中的电流强度的变化,T时可能加入了H2O2 | |
| D. | 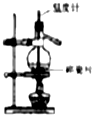 如图装置分离溴的四氯化碳溶液 |
9.下列“反应”中不是化学反应的是( )
| A. | 显色反应 | B. | 焰色反应 | C. | 颜色反应 | D. | 水解反应 |
10.a毫升A、B、C三种气态烃任意比的混合物跟足量氧气混合点燃后,恢复到原常温常压状态,气体体积共缩小了2.5a毫升,那么A、B、C三种烃可能是( )
| A. | CH4、C2H6、C3H8 | B. | C2H4、C2H6、CH4 | C. | CH4、C2H2、C2H6 | D. | C2H6、C3H6、C4H6 |
 现有一盛有无色固体物质M的试剂瓶,标签已破损(见图).
现有一盛有无色固体物质M的试剂瓶,标签已破损(见图).