题目内容
10.a毫升A、B、C三种气态烃任意比的混合物跟足量氧气混合点燃后,恢复到原常温常压状态,气体体积共缩小了2.5a毫升,那么A、B、C三种烃可能是( )| A. | CH4、C2H6、C3H8 | B. | C2H4、C2H6、CH4 | C. | CH4、C2H2、C2H6 | D. | C2H6、C3H6、C4H6 |
分析 设烃的混合物的平均化学式为CxHy,在氧气中燃烧的化学方程式为CxHy+(x+$\frac{y}{4}$)O2$\stackrel{点燃}{→}$xCO2+$\frac{y}{2}$H2O,根据体积变化,利用差量法计算.
解答 解:设烃的混合物的平均化学式为CxHy,混合物跟足量氧气混合点燃后,恢复到常温常压状态,水为液态,利用差量法计算,
CxHy+(x+$\frac{y}{4}$)O2$\stackrel{点燃}{→}$xCO2+$\frac{y}{2}$H2O△V
1 (x+$\frac{y}{4}$) x (1+$\frac{y}{4}$)
a 2.5a
即:$\frac{1}{a}=\frac{1+\frac{y}{4}}{2.5a}$;
解之得:y=6,即满足混合气体分子中平均含有6个H原子,
A.CH4、C2H6、C3H8混合气体平均H原子数目可能为6,不符合,故不A选;
B.C2H4、C2H6、CH4混合气体平均H原子数目小于6,不符合,故B不选;
C.CH4、C2H2、C2H6混合气体平均H原子数目小于6,符合,故C不选;
D.C2H6、C3H6、C4H6混合气体任意比平均H原子数目为6,符合,故D选,
故选D.
点评 本题考查混合物的有关计算,难度中等,注意差量法与平均值法的运用,侧重对学生思维能力的考查,注意若为任意比混合时,则各组分分子中H原子数目都是6.

练习册系列答案
 习题精选系列答案
习题精选系列答案
相关题目
20.NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 2.4g镁在二氧化碳中燃烧所转移的电子总数为0.2NA | |
| B. | 7.1g Cl2与足量NaOH(aq)反应时转移的电子总数为0.2 NA | |
| C. | 1 L1 mol/L的Na2CO3(aq)中CO32-与HCO3-的离子数之和为NA | |
| D. | 1 mol NaHSO4晶体中离子总数为3NA |
5.取m g的某物质在氧气中完全燃烧,所得产物跟足量的Na2O2固体完全反应.若Na2O2固体的质量增加m g,则下列物质中不能满足上述结果的是( )
| A. | CH3COOH | B. | H2 | C. | HCOOH | D. | CO |
15.已知某强氧化剂RO(OH)2+ 中的R元素被Na2SO3还原到低价态.如果还原2.4×10-3mol RO(OH)2+ 至较低价态,需要60 mL 0.1 mol/L的Na2SO3溶液.那么,R元素被还原成的价态是( )
| A. | -1 | B. | 0 | C. | +1 | D. | +2 |
2.已知某兴奋剂乙基雌烯醇(etylestrenol)的结构如图所示.下列叙述中正确的是( )


| A. | 该物质可以视为酚类 | B. | 该有机物的分子式为C19H32O | ||
| C. | 能使溴的四氯化碳溶液褪色 | D. | 该物质分子中的所有碳原子均共面 |
19.下列叙述中不正确的是( )
| A. | 糖类和蛋白质都是人体重要的营养物质 | |
| B. | 鸡蛋白可以水解得到氨基酸 | |
| C. | 液化石油气和天然气的主要成分都是甲烷 | |
| D. | 利用油脂在碱性条件下的水解,可以制得肥皂和甘油 |
7.乙烯等有机物间的转化关系如图所示,与此有关的说法正确的是( )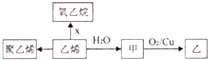

| A. | X为Cl2 | B. | 聚乙烯是纯净物 | ||
| C. | 甲与乙的含碳质量分数相同 | D. | CH3OCH3与甲互为同分异构体 |
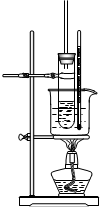 (1)试回答下列中学化学实验中常见仪器的有关问题:在仪器①分液漏斗、②试剂瓶、③集气瓶、④滴瓶、⑤滴定管、⑥容量瓶、⑦量筒、⑧托盘天平中,标有“0”刻度的是(填序号,下同)⑤⑧;标有使用温度的仪器是⑤⑥⑦.用到“磨砂”处理的有①②③④⑤⑥.
(1)试回答下列中学化学实验中常见仪器的有关问题:在仪器①分液漏斗、②试剂瓶、③集气瓶、④滴瓶、⑤滴定管、⑥容量瓶、⑦量筒、⑧托盘天平中,标有“0”刻度的是(填序号,下同)⑤⑧;标有使用温度的仪器是⑤⑥⑦.用到“磨砂”处理的有①②③④⑤⑥. .
.