题目内容
短周期元素X、Y、Z、W的原子序数依次增大,X原子的最外层电子数是其内层电子总数的3倍,Y原子的最外层只有2个电子,Z单质可制成半导体材料,W与X属于同一主族,下列叙述正确的是( )
| A、元素X的简单氢化物的沸点<元素W的简单氢化物的沸点 |
| B、元素W的最高价氧化物对应水化物的酸性比Z的弱 |
| C、化合物YX、ZX2、WX3中化学键的类型相同 |
| D、原子半径的大小顺序:rY>rZ>rW>rX |
考点:原子结构与元素周期律的关系
专题:
分析:短周期元素X、Y、Z、W的原子序数依次增大,X原子的最外层电子数是其内层电子总数的3倍,X有2个电子层,最外层电子数为6,故X为O元素;W与X属于同一主族,故W为S元素;Y原子的最外层只有2个电子,原子序数大于O元素,故Y处于第三周期,则Y为Mg元素;Z单质可制成半导体材料,Z为Si元素.
解答:
解:短周期元素X、Y、Z、W的原子序数依次增大,X原子的最外层电子数是其内层电子总数的3倍,X有2个电子层,最外层电子数为6,故X为O元素;W与X属于同一主族,故W为S元素;Y原子的最外层只有2个电子,原子序数大于O元素,故Y处于第三周期,则Y为Mg元素;Z单质可制成半导体材料,Z为Si元素,
A.由于水分子之间存在氢键,故水的沸点高于硫化氢,故A错误;
B.非金属Si<S,故酸性硅酸<硫酸,故B错误;
C.化合物MgO为离子化合物,含有离子键,SiO2、SO3属于共价化合物,含有共价键,故C错误;
D.同周期自左而右原子半径减小,同主族电子层越多原子半径越大,故原子半径Mg>Si>S>O,即rY>rZ>rW>rX,故D正确;
故选D.
A.由于水分子之间存在氢键,故水的沸点高于硫化氢,故A错误;
B.非金属Si<S,故酸性硅酸<硫酸,故B错误;
C.化合物MgO为离子化合物,含有离子键,SiO2、SO3属于共价化合物,含有共价键,故C错误;
D.同周期自左而右原子半径减小,同主族电子层越多原子半径越大,故原子半径Mg>Si>S>O,即rY>rZ>rW>rX,故D正确;
故选D.
点评:本题考查结构性质与位置关系、元素周期律等,难度不大,推断元素是解题的关键,注意对元素周期律的理解掌握.

练习册系列答案
相关题目
下列离子方程式不正确的是 ( )
| A、铁桶被稀盐酸腐蚀:Fe+2H+═Fe2++H2 ↑ |
| B、常温下氯气与烧碱溶液反应:Cl2+2OH-═Cl-+ClO-+H2O |
| C、硫酸钠溶液与氢氧化钡溶液反应:Ba2++SO42-═BaSO4↓ |
| D、氯气融入碘化钾溶液:Cl2 +I-═Cl-+I2 |
电子表所用的纽扣电池的两极材料为锌和氧化银,电解质溶液为KOH溶液,其电极反应式是:Zn+2OH--2e-═ZnO+H2O:Ag2O+H2O+2e-═2Ag+2OH-.总反应式为:Ag2O+Zn═2Ag+ZnO,下列说法正确的是( )
| A、Zn为正极,Ag2O为负极 |
| B、电解质溶液中,OH-移向Ag2O极 |
| C、原电池工作时,正极区溶液pH值增大 |
| D、原电池工作时,负极区溶液pH值增大 |
能正确表示下列反应的离子方程式是( )
| A、在碳酸氢钠溶液中加入盐酸:HCO3-+H+=CO2↑+H2O |
| B、把金属铁放入稀硫酸中:2Fe+6H+=2Fe3++3H2↑ |
| C、向氯化亚铁溶液中通入氯气:Fe2++Cl2=Fe3++2Cl- |
| D、钠跟水反应:Na+2H2O=Na++2OH-+H2↑ |
向含溶质0.2mol的Al2(SO4)3溶液中加入1000mL KOH溶液,生成白色沉淀7.8g,则KOH溶液的物质的量浓度可能为( )
| A、0.3mol/L |
| B、0.7mol/L |
| C、0.8 mol/L |
| D、1.5mol/L |
两种金属的混合物15g,溶于足量稀H2SO4,生成氢气0.5mol.则混合物不可能是( )
| A、Cu和Mg |
| B、Zn和Fe |
| C、Na和Al |
| D、Al和Fe |
用1L 1.0mol?L-1 NaOH溶液吸收17.92L CO2(标况下),所得溶液中的CO32-和HCO3-的物质的量浓度之比约是( )
| A、1:3 | B、1:2 |
| C、2:3 | D、3:2 |
 +Zn→CH2=CH2+ZnBr2.写出以1,3-丁二烯为原料合成高分子化合物
+Zn→CH2=CH2+ZnBr2.写出以1,3-丁二烯为原料合成高分子化合物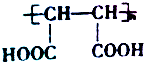 的流程图.
的流程图.