题目内容
用NA表示阿伏伽德罗常数的值,下列说法正确的是( )
| A、在常温常压下,11.2L H2含有的分子数为0.5NA |
| B、32g O2所含原子数目为2NA |
| C、1mol HCl含有的电子数为2NA |
| D、在标准状况下,22.4L H2O含有的质子数为10NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、根据在常温下,不是标准状况下进行判断;
B、根据n=
计算出氧气的物质的量,计算出含有的氧原子数目;
C、根据1mol氯化氢中含有18mol电子判断;
D、根据标准状况下水的状态不是气体判断.
B、根据n=
| m |
| M |
C、根据1mol氯化氢中含有18mol电子判断;
D、根据标准状况下水的状态不是气体判断.
解答:
解:A、不是标准状况下,题中条件无法计算11.2L氢气的物质的量,故A错误;
B、32g氧气的物质的量为1mol,1mol氧气含有2mol氧原子,所含原子数目为2NA,故B正确;
C、1mol氯化氢中含有18mol电子,含有的电子数为18NA,故C错误;
D、标准状况下,水不是气体,不能使用标准状况下的气体摩尔体积计算22.4L水的物质的量,故D错误;
故选B.
B、32g氧气的物质的量为1mol,1mol氧气含有2mol氧原子,所含原子数目为2NA,故B正确;
C、1mol氯化氢中含有18mol电子,含有的电子数为18NA,故C错误;
D、标准状况下,水不是气体,不能使用标准状况下的气体摩尔体积计算22.4L水的物质的量,故D错误;
故选B.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意标准状况下水、四氯化碳、三氧化硫等不是气体,阿伏加德罗常数是高考的“热点”,它既考查了学生对物质的量、粒子数、质量、体积等与阿伏加德罗常数关系的理解,又可以涵盖多角度的化学知识内容.要准确解答好这类题目,一是要掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系;二是要准确弄清分子、原子、原子核内质子中子及核外电子的构成关系.

练习册系列答案
相关题目
在下列溶液中,各组离子一定能够大量共存的是( )
| A、硫氰化钾溶液:Na+、Cl-、SO42-、Fe3+ |
| B、使紫色石蕊试液变红的溶液:Fe2+、Mg2+、ClO-、Cl- |
| C、氢氧化钠溶液:K+、Ba2+、Cl-、Br- |
| D、碳酸钠溶液:K+、SO42-、Cl-、H+ |
下列反应的离子方程式正确的是( )
| A、铜片加入三氯化铁溶液中:Cu+2Fe3+═2Fe2++Cu2+ |
| B、盐酸中加入碳酸钙:CO32-+2H+═H2O+CO2↑ |
| C、AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ |
| D、NaHCO3溶液中加入盐酸:CO32-+2H+═H2O+CO2↑ |
下列对有关化学反应过程或实验现象的解释中,正确的是( )
| A、Cl2的水溶液可以导电,说明Cl2是电解质 |
| B、在高温条件下,C能置换出SiO2中的Si,说明C的氧化性强于Si |
| C、向淀粉碘化钾的溶液中加入氯水,溶液变为蓝色,说明Cl2的氧化性强于I2 |
| D、在滴有酚酞的Na2CO3溶液中,加入BaCl2溶液,溶液褪色,说明BaCl2溶液有酸性 |
100mL 1.2mol/L AlCl3溶液与一定量2.0mol/L NaOH溶液混合后,得到7.8g沉淀,则所加NaOH溶液的体积是( )
| A、150mL |
| B、190mL |
| C、150mL或190mL |
| D、180mL |
 同学们为了探究镁条与盐酸、醋酸反应时,浓度或温度对反应速率(观察镁条消失的时间)的影响,他们准备了以下化学用品:0.2mol/L与0.40mol/L的HCl溶液、0.2mol/L与0.40mol/L的CH3COOH溶液、4条镁条(形状、大小、质量相同)、几支试管和胶头滴管,酸液温度控制为298K和308K.
同学们为了探究镁条与盐酸、醋酸反应时,浓度或温度对反应速率(观察镁条消失的时间)的影响,他们准备了以下化学用品:0.2mol/L与0.40mol/L的HCl溶液、0.2mol/L与0.40mol/L的CH3COOH溶液、4条镁条(形状、大小、质量相同)、几支试管和胶头滴管,酸液温度控制为298K和308K. 物质A~G均由短周期元素组成,A、B为非金属气体单质,B原子最外层电子数比次外层电子数的2倍还多1.甲、乙均为金属单质,且甲的原子半径在第三周期最大.各物质间的转化关系如下(部分生成物未给出,且未注明反应条件):请回答:
物质A~G均由短周期元素组成,A、B为非金属气体单质,B原子最外层电子数比次外层电子数的2倍还多1.甲、乙均为金属单质,且甲的原子半径在第三周期最大.各物质间的转化关系如下(部分生成物未给出,且未注明反应条件):请回答: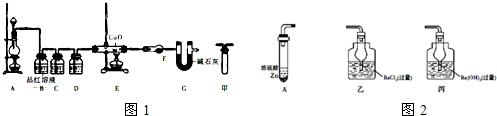
 (1)已知:N≡N的键能是946kJ/mol,H-H的键能为436kJ/mol,N-H的键能为391kJ/mol,请根据此次而出合成氨反应的热化学方程式
(1)已知:N≡N的键能是946kJ/mol,H-H的键能为436kJ/mol,N-H的键能为391kJ/mol,请根据此次而出合成氨反应的热化学方程式