题目内容
由C、H、O组成的化合物5.80毫克,完全燃烧后得到CO213.2毫克,H2O5.4毫克.则该化合物的化学式是( )
| A、C3H8O2 |
| B、C2H4O |
| C、C5H10O2 |
| D、C3H6O |
考点:有关有机物分子式确定的计算
专题:烃及其衍生物的燃烧规律
分析:根据有机物燃烧生成二氧化碳、水的质量计算出碳元素、氢元素的物质的量、质量,根据质量守恒计算出氧原子的质量、物质的量,从而可以计算出该有机物的最简式,然后对各选项进行判断即可.
解答:
解:5.80毫克二氧化碳的物质的量为:n(CO2)=
=3×10-4mol,含有碳原子质量为:m(C)=12g/mol×3×10-4mol=3.6×10-3g,
5.4毫克水的物质的量为:n(H2O)=
=3×10-4mol,3×10-4mol水中含有6×10-4molH原子,含氢元素的质量为:1g/mol×6×10-4mol=6×10-4g,
5.80毫克该化合物中含有氧原子的质量为:5.8×10-3g-3.6×10-3g-6×10-4g=1.6×10-3g,含有的O原子的物质的量为:n(O)=
=1×10-4mol,
该有机物分子中含有的C、H、O原子的物质的量之比为3×10-4mol:6×10-4mol:1×10-4mol=3:6:1,
该有机物的最简式为:C3H6O,由于H原子已经达到饱和,则其最简式就是其分子式:C3H6O,
故选D.
| 13.2×10-3g |
| 44g/mol |
5.4毫克水的物质的量为:n(H2O)=
| 5.4×10-3g |
| 18g/mol |
5.80毫克该化合物中含有氧原子的质量为:5.8×10-3g-3.6×10-3g-6×10-4g=1.6×10-3g,含有的O原子的物质的量为:n(O)=
| 1.6×10-3g |
| 16g/mol |
该有机物分子中含有的C、H、O原子的物质的量之比为3×10-4mol:6×10-4mol:1×10-4mol=3:6:1,
该有机物的最简式为:C3H6O,由于H原子已经达到饱和,则其最简式就是其分子式:C3H6O,
故选D.
点评:本题考查了有机物分子式的计算,题目难度中等,注意掌握确定有机物分子式、结构简式的常用方法,特别是根据质量守恒确定有机物中含有氧元素的量为解答本题的关键.

练习册系列答案
相关题目
将盛满NO2和O2混合气体的试管倒立于水中,经过足够长的时间后,试管内气体体积缩小为原体积的一半,则剩余气体的成分是( )
| A、NO或O2 |
| B、NO |
| C、O2 |
| D、NO2 |
取含有 0.02mol 的硫酸溶液,先投入 0.24g 镁粉,再滴入NaOH 溶液,当使溶液中的镁离子全部转化为沉淀时,需要NaOH的物质的量为( )
| A、0.02mol |
| B、0.03mol |
| C、0.04mol |
| D、0.01mol |
某位同学配制一定物质的量浓度的NaOH溶液时,造成所配溶液浓度偏高的原因是( )
| A、所用NaOH已潮解 |
| B、用带游码的托盘天平称2.4gNaOH时误用了“左码右物”方法 |
| C、有少量NaOH溶液残留在烧杯里 |
| D、向容量瓶中加水未到刻度线 |
下列实验装置正确且能达到实验目的是( )
A、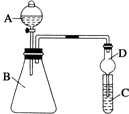 证明非金属性氯>碳>硅(A、B、C中的试剂分别为盐酸、石灰石和硅酸钠溶液) |
B、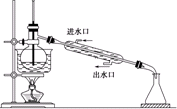 石油分馏 |
C、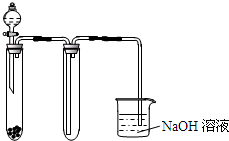 用KMnO4与浓盐酸反应制取适量氯气的简易装置 |
D、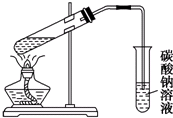 实验室制乙酸乙酯 |
下列金属单质中,不能从CuCl2溶液中置换出铜的是( )
| A、锌 | B、镁 | C、钠 | D、铁 |
下列实验装置或操作正确的是( )
A、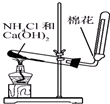 制取氨气 |
B、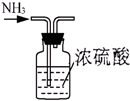 干燥氨气 |
C、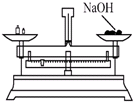 称量NaOH固体 |
D、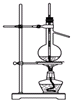 石油的分馏 |
下列叙述正确的是( )
| A、合成氨工业中为了提高氢气利用率,适当增加氢气浓度 |
| B、Mg、Al、Cu可以分别用置换法、直接加热法和电解法冶炼得到 |
| C、蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质 |
| D、电解饱和食盐水制烧碱采用离子交换膜法,可防止阴极室生产的Cl2进入阳极室 |