题目内容
下列实验操作、现象和结论均正确的是( )
| 操作 | 现象 | 结论 | |
| A | 向某溶液中加入1毫升四氯化碳,振荡,静置 | 上层溶液显紫色 | 原溶液中有碘单质 |
| B | 向某溶液中滴加稀氢氧化钠溶液,将湿润的红色石蕊试纸置试管口 | 试纸不变蓝 | 原溶液中无铵根 |
| C | 将干燥的淀粉-碘化钾试纸靠近导管口 | 试纸不变蓝 | 无氯分子 |
| D | 向某溶液中滴加硝酸银和稀硝酸溶液 | 生成浅黄色沉淀 | 原溶液中有溴离子 |
| A、A | B、B | C、C | D、D |
考点:化学实验方案的评价
专题:实验评价题
分析:A.四氯化碳的密度比水大;
B.滴加稀氢氧化钠溶液,加热,试纸不变蓝,说明原溶液中无铵根离子;
C.试纸测定气体应润湿;
D.溴化银是浅黄色沉淀.
B.滴加稀氢氧化钠溶液,加热,试纸不变蓝,说明原溶液中无铵根离子;
C.试纸测定气体应润湿;
D.溴化银是浅黄色沉淀.
解答:
解:A.四氯化碳的密度比水大,下层呈紫红色,故A错误;
B.氨气极易溶于水,若溶液中含有少量的NH4+时,滴加稀NaOH溶液不会放出NH3,故B错误;
C.淀粉碘化钾试纸应润湿,故C错误;
D.有浅黄色沉淀,说明原溶液中有溴离子,故D正确.
故选D.
B.氨气极易溶于水,若溶液中含有少量的NH4+时,滴加稀NaOH溶液不会放出NH3,故B错误;
C.淀粉碘化钾试纸应润湿,故C错误;
D.有浅黄色沉淀,说明原溶液中有溴离子,故D正确.
故选D.
点评:本题考查离子的检验,要掌握常见离子的检验方法,注意排除其它离子的干扰,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
类比推断是学习化学的一种重要方法.下列推断正确的是( )
| A、NO和NO2的密度都比空气大,都可以用向上排空气法收集 |
| B、丙烷和乙醇的分子量相近,二者沸点也相近 |
| C、SO2和CO2都是酸性氧化物,都能与KOH溶液反应 |
| D、Na2O和Na2O2所含元素相同,故与CO2反应产物也相同 |
在给定条件的水溶液中一定能大量共存的离子组是( )
| A、含有SO42-的溶液:Ca2+、NH4+、HCO3-、Cl- |
| B、c(Fe2+)=0.5 mol/L的溶液:H+、Na+、Cl-、SO42- |
| C、pH=1的溶液:Na+、K+、Cl-、CO32- |
| D、酸性无色透明溶液中:Fe2+、Na+、NO3-、CO32- |
下列说法正确的是( )
A、按系统命名法,化合物 的名称为2,4-二乙基-6-丙基辛烷 的名称为2,4-二乙基-6-丙基辛烷 |
B、DDT的结构简式为 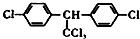 ,分子中最多有14个碳原子共平面 ,分子中最多有14个碳原子共平面 |
| C、醋酸和硬脂酸互为同系物,C2H6和C9H20也一定互为同系物 |
D、结构片段为 的高聚物,是其单体通过缩聚反应生成 的高聚物,是其单体通过缩聚反应生成 |
下列实验操作或装置符合实验要求的是( )
A、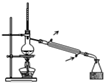 用如图装置可用于分离互不相溶的液体 |
B、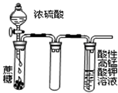 用如图装置酸性KMnO4溶液中没有气泡出现,但溶液颜色会逐渐变浅乃至褪去 |
C、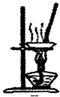 用如图所示装置蒸干NH4Cl饱和溶液制备NH4Cl晶体 |
D、 用如图确认CO2和NaOH已发生反应 |
以NA表示阿伏加德罗常数,下列说法中正确的是( )
| A、1.8g NH4+离子中含有的电子数为NA |
| B、常温常压下,1mol甲基(-CH3)所含电子数为10NA |
| C、25℃,1.01×105 Pa下,使V L氯化氢气体溶于水得V L水溶液,所得溶液的物质的量浓度为1/22.4 mol?L-1 |
| D、标准状况下,22.4 L Cl2和HCl的混合气体中含分子总数为2NA |
由C、H、O组成的化合物5.80毫克,完全燃烧后得到CO213.2毫克,H2O5.4毫克.则该化合物的化学式是( )
| A、C3H8O2 |
| B、C2H4O |
| C、C5H10O2 |
| D、C3H6O |
对A2+3B2?2AB3反应来说,以下反应速率的表示,最快的是( )
| A、VA2=0.4mol?L-1?min-1 |
| B、VB2=0.6mol?L-1?min-1 |
| C、VAB3=0.5mol?L-1?min-1 |
| D、无法判断 |