题目内容
9.下列元素中,属于第ⅠA族的是( )| A. | Mg | B. | P | C. | Li | D. | S |
分析 在原子结构中,最外层电子数=主族元素的族序数,以此来解答.
解答 解:A.镁的最外层电子数为2,位于第ⅡA族,故A不选;
B.磷的最外层电子数为5,位于ⅤA族,故B不选;
C.Li的最外层电子数为1,位于第IA族,故C选;
D.S的最外层电子数为6,位于第ⅤⅠA族,故D不选;
故选C.
点评 本题考查元素周期表的结构及应用,为高频考点,把握原子结构与元素的位置为解答的关键,注意常见的主族元素与副族元素,注重基础知识的考查,题目难度不大.

练习册系列答案
 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案
相关题目
19.下列物质中所有原子均满足最外层8电子稳定结构的化合物是( )
| A. | PCl5 | B. | P4 | C. | CCl4 | D. | NH3 |
17. 以铬铁矿(主要成分FeO•Cr2O3,含有少量SiO2等)为原料制取铬酸钠晶体(Na2CrO4)工艺流程如图所示.
以铬铁矿(主要成分FeO•Cr2O3,含有少量SiO2等)为原料制取铬酸钠晶体(Na2CrO4)工艺流程如图所示.
已知:①酸性溶液中Cr的+6价易被还原为+3价;当pH>9时Cr以CrO2-形式存在且易被氧化;
②常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下:
(1)滤渣a的主要成分的化学式是SiO2;操作X用到的玻璃仪器有烧杯、玻璃棒、和漏斗.
(2)第④步得到产品涉及到的操作有蒸发浓缩、降温结晶、过滤、洗涤等.
(3)第①步反应的离子方程式是FeO+2H+=Fe2++H2O、Cr2O3+6H+=2Cr3++3H2O,第②步产生滤渣b的原因是Fe3+水解生成氢氧化铁沉淀.
(4)已知:1molAl完全燃烧放热a KJ,1mol Fe完全燃烧生成Fe3O4放热b KJ,写出Al与Fe3O4发生铝热反应的热化学方程式8Al(s)+3Fe3O4 (s)=9Fe(s)+4Al2O3 (s),△H=(8a-9b)kJ/mol.
(5)若现有224kg铬铁矿(其中含FeO•Cr2O3 50%),按上述流程最多可以得到Na2CrO4产品的质量是189kg(假设每步均恰好完全转化).
 以铬铁矿(主要成分FeO•Cr2O3,含有少量SiO2等)为原料制取铬酸钠晶体(Na2CrO4)工艺流程如图所示.
以铬铁矿(主要成分FeO•Cr2O3,含有少量SiO2等)为原料制取铬酸钠晶体(Na2CrO4)工艺流程如图所示.已知:①酸性溶液中Cr的+6价易被还原为+3价;当pH>9时Cr以CrO2-形式存在且易被氧化;
②常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下:
| 阳离子 | Fe3+ | Fe2+ | Cr3+ |
| 开始沉淀时的pH | 2.7 | 7.6 | |
| 沉淀完全的pH | 3.7 | 9.6 | 9(>9)溶解 |
(2)第④步得到产品涉及到的操作有蒸发浓缩、降温结晶、过滤、洗涤等.
(3)第①步反应的离子方程式是FeO+2H+=Fe2++H2O、Cr2O3+6H+=2Cr3++3H2O,第②步产生滤渣b的原因是Fe3+水解生成氢氧化铁沉淀.
(4)已知:1molAl完全燃烧放热a KJ,1mol Fe完全燃烧生成Fe3O4放热b KJ,写出Al与Fe3O4发生铝热反应的热化学方程式8Al(s)+3Fe3O4 (s)=9Fe(s)+4Al2O3 (s),△H=(8a-9b)kJ/mol.
(5)若现有224kg铬铁矿(其中含FeO•Cr2O3 50%),按上述流程最多可以得到Na2CrO4产品的质量是189kg(假设每步均恰好完全转化).
4.常温下aLpH=3的二元弱酸H2R溶液与aLpH=11的NaOH溶液混合后,混合液的pH刚好等于7(液体反应的后体积不变);则对反应后混合液的叙述正确的是( )
| A. | c(R2-)+c(OH-)=c(Na+)+c(H+) | B. | c(R2-)>c(Na+)>c(H+)=c(OH-) | ||
| C. | 2c(R2-)+c(HR-)=c(Na+) | D. | 混合后溶液的体积为2aL |
14.图为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题:

(1)②是C.
(2)9种元素中非金属性最强的是F.
(3)④⑥⑦的原子半径由小到大的顺序为O<Al<Na.
(4)②③⑧的最高价含氧酸的酸性由弱到强的顺序是H2SiO3<H2CO3<HNO3.
(5)由以上某些元素组成的有机化合物 ,其分子式是C9H10O3,含氧官能团的名称是:羧基、醇羟基.
,其分子式是C9H10O3,含氧官能团的名称是:羧基、醇羟基.
(6)某化学兴趣小组为探究⑨单质、Br2、Fe3+的氧化性强弱,设计了如下实验:
①整套实验装置存在一处明显的不足,请指出缺少尾气处理装置.
②用改正后的装置进行实验,实验过程如下:

(1)②是C.
(2)9种元素中非金属性最强的是F.
(3)④⑥⑦的原子半径由小到大的顺序为O<Al<Na.
(4)②③⑧的最高价含氧酸的酸性由弱到强的顺序是H2SiO3<H2CO3<HNO3.
(5)由以上某些元素组成的有机化合物
 ,其分子式是C9H10O3,含氧官能团的名称是:羧基、醇羟基.
,其分子式是C9H10O3,含氧官能团的名称是:羧基、醇羟基.(6)某化学兴趣小组为探究⑨单质、Br2、Fe3+的氧化性强弱,设计了如下实验:

①整套实验装置存在一处明显的不足,请指出缺少尾气处理装置.
②用改正后的装置进行实验,实验过程如下:
| 实验操作 | 实验现象 | 结论 |
| 打开活塞a,向圆底烧瓶中滴入适量浓盐酸;然后关闭活塞a,点燃酒精灯. | D装置中:溶液变红 E装置中:水层溶液变黄,振荡后,CCl4层无明显变化,持续通入一段时间后,CCl4层变为棕色 | ⑨单质、Br2、Fe3+的氧化性由强到弱的顺序是: ⑨单质(或Cl2)>Br2>Fe3+ |
18.下列物质中,含氢原子数目最多的是( )
| A. | 0.9 mol H2O | B. | 0.3 mol H2SO4 | C. | 0.2 mol NH3 | D. | 0.4 mol CH4 |

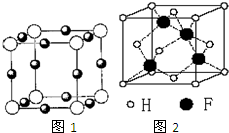 已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E<F.其中A原子核外有三个未成对电子;化合物B2E的晶体为离子晶体,E原子核外的M层中只有两对成对电子;C元素是地壳中含量最高的金属元素;D单质的晶体类型在同周期的单质中没有相同的;F原子核外最外层电子数与B相同,其余各层电子均充满.请根据以上信息,回答下列问题:(答题时,A、B、C、D、E、F用所对应的元素符号表示)
已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E<F.其中A原子核外有三个未成对电子;化合物B2E的晶体为离子晶体,E原子核外的M层中只有两对成对电子;C元素是地壳中含量最高的金属元素;D单质的晶体类型在同周期的单质中没有相同的;F原子核外最外层电子数与B相同,其余各层电子均充满.请根据以上信息,回答下列问题:(答题时,A、B、C、D、E、F用所对应的元素符号表示)