题目内容
发射卫星的火箭推进器中大多使用燃料偏二甲肼,其化学式C2H8N2.计算:
(1)偏二甲肼的摩尔质量是 ;480g偏二甲肼的物质的量为 .
(2)偏二甲肼中碳原子与氮原子的个数之比是 ,其物质的量之比是 ;1mol偏二甲肼中含有的氢原子数目是 .
(1)偏二甲肼的摩尔质量是
(2)偏二甲肼中碳原子与氮原子的个数之比是
考点:物质的量的相关计算
专题:计算题
分析:(1)摩尔质量以g/mol为单位,数值上等于其相对分子质量,根据n=
计算480g偏二甲肼的物质的量;
(2)根据化学式确定偏二甲肼中碳原子与氮原子的个数之比、物质的量之比;H原子物质的量为偏二甲肼的8倍,再根据N=nNA计算H原子数目.
| m |
| M |
(2)根据化学式确定偏二甲肼中碳原子与氮原子的个数之比、物质的量之比;H原子物质的量为偏二甲肼的8倍,再根据N=nNA计算H原子数目.
解答:
解:(1)C2H8N2的相对分子质量为60,故其摩尔质量为60g/mol,480g偏二甲肼的物质的量为
=8mol,故答案为:60g/mol;8mol;
(2)根据偏二甲肼化学式C2H8N2,可知碳原子与氮原子的个数之比2:2=1:1、C、N原子物质的量之比为1:1;H原子物质的量为偏二甲肼的8倍,1mol偏二甲肼含有H原子数目=1mol×8×NAmol-1=8NA,
故答案为:1:1;1:1;8NA.
| 480g |
| 60g/mol |
(2)根据偏二甲肼化学式C2H8N2,可知碳原子与氮原子的个数之比2:2=1:1、C、N原子物质的量之比为1:1;H原子物质的量为偏二甲肼的8倍,1mol偏二甲肼含有H原子数目=1mol×8×NAmol-1=8NA,
故答案为:1:1;1:1;8NA.
点评:本题考查物质的量有关计算、化学式意义等,比较基础,注意对基础知识的理解掌握.

练习册系列答案
相关题目
0.5L的Fe2(SO4)3溶液中Fe3+的浓度为0.2mol/L,与0.2L0.5mol/L的Na2SO4溶液中SO42-的浓度之比是( )
| A、3:2 | B、2:5 |
| C、3:5 | D、5:3 |
如图示装置是化学实验室的常用装置,它有多种用途.以下各项用途的操作都正确的是( )


| A、洗气或干燥装置:瓶内放一定体积溶液,由a进气 |
| B、用于收集氢气:瓶内充满水,由b进气 |
| C、排空气收集H2:瓶内充满空气,由a进气 |
| D、病人输氧时用于观察输氧速度:瓶内装适量水,b接病人鼻腔 |
0.3mol硼烷(B2H6)在氧气中完全燃烧生成B2O3固体和液态水,放出649.5kJ热量.下列判断正确的是( )
| A、该反应是非氧化还原反应 |
| B、在理论上可以利用该反应的原理做成燃料电池 |
| C、该反应的热化学方程式为:B2H6(g)+3O2(g)═B2O3(s)+3H2O(l)△H=2 165 kJ?mol-1 |
| D、每生成18 g水,该反应转移2 mol电子 |
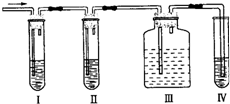 某混合气体可能是乙烯和二氧化硫的混合气,有人设计下列实验图以确认上述混合气体中有CH2=CH2和SO2.Ⅰ、Ⅱ、Ⅲ、Ⅳ装置中盛放的试剂依次是:品红溶液、NaOH溶液、品红溶液、酸性KMnO4溶液.回答下列问题:
某混合气体可能是乙烯和二氧化硫的混合气,有人设计下列实验图以确认上述混合气体中有CH2=CH2和SO2.Ⅰ、Ⅱ、Ⅲ、Ⅳ装置中盛放的试剂依次是:品红溶液、NaOH溶液、品红溶液、酸性KMnO4溶液.回答下列问题: 甲、乙、丙、丁四种物质转化关系如图.已知甲是地壳中含量最高的元素组成的单质.
甲、乙、丙、丁四种物质转化关系如图.已知甲是地壳中含量最高的元素组成的单质.