题目内容
9.下列有关物质除杂的方法中可行的是( )| A. | 除去石英中混有的少量铝粉,可加入氢氧化钠溶液溶解后过滤 | |
| B. | 向含少量FeBr2的FeCl2溶液中,加入适量氯水,再加CCl4萃取,以除去FeCl2溶液中的FeBr2 | |
| C. | 除去乙酸乙酯中混有的少量乙酸,加入饱和氢氧化钠溶液振荡后分液 | |
| D. | 除去CuCl2溶液中混有的少量FeCl3,可向溶液中加入CuO后再过滤 |
分析 A.石英、铝均能与NaOH溶液反应;
B.氯水先氧化亚铁离子,再氧化溴离子;
C.乙酸乙酯、乙酸均与NaOH溶液反应;
D.加入CuO可增大溶液pH,有利于铁离子的水解.
解答 解:A.因石英、铝均能与NaOH溶液反应,则除去石英中混有的少量铝粉,可加入足量盐酸溶解后过滤,故A错误;
B.因氯水先氧化亚铁离子,再氧化溴离子,向含有少量的FeBr2的FeCl2溶液中,应先加入足量氯水,再加足量铁粉,最后加CC14萃取分液,以除去FeC12溶液中的FeBr2,故B错误;
C.乙酸乙酯、乙酸均与NaOH溶液反应,除去乙酸乙酯中混有的少量乙酸,应加入饱和碳酸钠溶液振荡后分液,故C错误;
D.加入CuO可增大溶液pH,有利于铁离子的水解,可用于除杂,故D正确.
故选D.
点评 本题考查混合物的分离、提纯,为高频考点,侧重于学生的分析、实验能力的考查,注意除杂时既要除去杂质还不能引入新的杂质,不能使被除杂的物质发生反应,明确物质的性质是解答本题的关键,选项D为解答的难点,题目难度中等.

练习册系列答案
相关题目
3.常温下,已知 H2S-HS--S2-和H2SO3-HSO3--SO32-粒子体系随pH变化时各组分的分布情况如图1所示.现向1L0.1mol•L-1的Na2S溶液中缓慢通入SO2气体,溶液的pH与通入SO2的物质的量变化的关系如图2所示.下列说法不正确的是( )
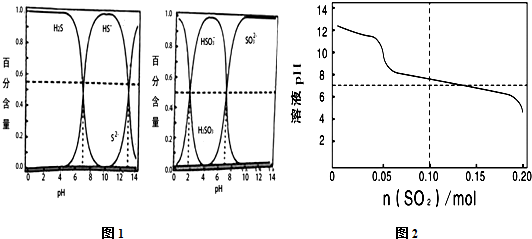

| A. | 由图1的一级电离与二级电离的Ka值可知H2SO3?2H++SO32- Ka≈10-7 | |
| B. | 向1L0.1 mol•L-1的Na2S溶液中持续通入SO2气体达到0.1 mol时,溶液中H2S、HS-、HSO3-、SO32-可同时一定量共存 | |
| C. | 向1L0.1 mol•L-1的Na2S溶液中持续通入SO2气体达到0.1 mol时,溶液中存在如下关系:c(H+)+c(Na+)═c(OH-)+2c(S2-)+2c(SO32-)+c(HS- )+c(HSO3-) | |
| D. | 在反应过程中当pH降至7.5左右,之后可能出现淡黄色沉淀 |
4.在强酸性溶液中能大量共存,并且溶液为无色透明的离子组是( )
| A. | NH4+、Al3+、SO42-、NO3- | B. | K+、Na+、S2-、Cl- | ||
| C. | K+、NH4+、MnO4-、SO42- | D. | Na+、K+、NO3-、HCO3- |
4.市场销售的某种食用精制盐包装袋上有如下说明:
(1)碘酸钾与碘化钾在酸性条件下发生如下反应,配平离子方程式(将化学计量数填于空白处)
1IO3-+5I-+6H+=3I2+3H2O
(2)上述反应生成的I2可用四氯化碳检验.向碘的四氯化碳溶液中加入Na2SO3稀溶液,将I2还原,以回收四氯化碳.
①Na2SO3稀溶液与I2反应的离子方程式是I2+SO32-+H2O=2I-+SO42-+2H+.
②某学生设计回收四氯化碳的操作步骤为:
a.将碘的四氯化碳溶液置于分液漏斗中;b.加入适量Na2SO3稀溶液;c.分离出下层液体.
以上设计中遗漏的操作及在上述步骤中的位是在步骤b后,增加操作;
所缺步骤为将分液漏斗充分振荡后静置
(3)已知:I2+2S2O32-=2I-+S4O62-.某学生测定食用精制盐的碘含量,其步骤为:
a.准确称取12.7g食盐,加适量蒸馏水使其完全溶解;
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全;
c.以淀粉为指示剂,逐滴加入物质的量浓度为6.0×10-4mol•L-1的Na2S2O3溶液20.0mL,恰好反应完全.
①判断c中反应恰好完全依据的现象是滴入最后一滴溶液时,溶液的蓝色恰好消失,且半分钟内不恢复原色,则达到滴定终点.
②根据以上实验和包装袋说明,所测精制盐的碘含量是20 mg/kg.
| 产品标准 | GB5461 |
| 产品等级 | 一级 |
| 配 料 | 食盐、碘酸钾、抗结剂 |
| 碘含量(以I计) | 20~50mg/kg |
1IO3-+5I-+6H+=3I2+3H2O
(2)上述反应生成的I2可用四氯化碳检验.向碘的四氯化碳溶液中加入Na2SO3稀溶液,将I2还原,以回收四氯化碳.
①Na2SO3稀溶液与I2反应的离子方程式是I2+SO32-+H2O=2I-+SO42-+2H+.
②某学生设计回收四氯化碳的操作步骤为:
a.将碘的四氯化碳溶液置于分液漏斗中;b.加入适量Na2SO3稀溶液;c.分离出下层液体.
以上设计中遗漏的操作及在上述步骤中的位是在步骤b后,增加操作;
所缺步骤为将分液漏斗充分振荡后静置
(3)已知:I2+2S2O32-=2I-+S4O62-.某学生测定食用精制盐的碘含量,其步骤为:
a.准确称取12.7g食盐,加适量蒸馏水使其完全溶解;
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全;
c.以淀粉为指示剂,逐滴加入物质的量浓度为6.0×10-4mol•L-1的Na2S2O3溶液20.0mL,恰好反应完全.
①判断c中反应恰好完全依据的现象是滴入最后一滴溶液时,溶液的蓝色恰好消失,且半分钟内不恢复原色,则达到滴定终点.
②根据以上实验和包装袋说明,所测精制盐的碘含量是20 mg/kg.
1.下列事实不能用平衡移动原理解释的是( )
| A. |  开启啤酒 | B. |  双氧水中加入氯化铁 | ||
| C. |  合成氨时增压 | D. |  NO2置于热水和冰水中 |
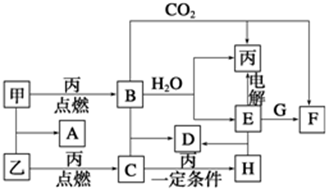
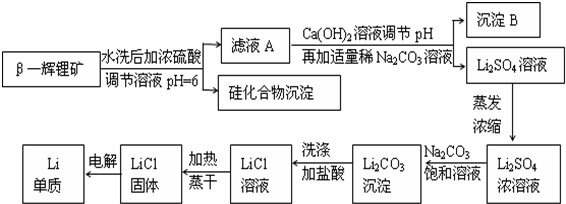
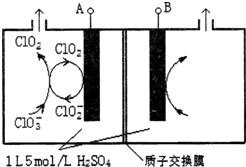 二氧化氯(ClO2)是国内外公认的高效、广谱、快速、安全无毒的杀菌消毒剂,被称为“第4代消毒剂”.工业上可采用氯酸钠(NaClO3)或亚氯酸钠(NaClO2)为原料制备ClO2.
二氧化氯(ClO2)是国内外公认的高效、广谱、快速、安全无毒的杀菌消毒剂,被称为“第4代消毒剂”.工业上可采用氯酸钠(NaClO3)或亚氯酸钠(NaClO2)为原料制备ClO2.