题目内容
现有A、B、C、D、E五种可溶性强电解质,它们在水中可电离产生下列离子(各离子不重复):阳离子:H+、Na+、Al3+、Ag+、Ba2+ 阴离子:OH-、Cl-、CO32-、NO3-、SO42-
已知:
①A、B两溶液呈碱性,C、D、E溶液呈酸性.
②向E溶液中逐滴滴加B溶液至过量,沉淀量先增加后减少但不消失.
③D溶液与另外四种溶液反应都能产生沉淀.
请回答下列问题:
(1)写出A与D的化学式:A ,D .
(2)写出A与E溶液反应的离子方程式: .
(3)已知:NaOH(aq)+HNO3(aq)═NaNO3(aq)+H2O(l)△H=-akJ?mol-1.请写出表示相同条件下B与C的稀溶液反应的中和热的热化学方程式: .
(4)若25℃时,C、E及醋酸三种溶液的pH=4,则E和C溶液中由水电离出的c(H+)的比是 ;将C与醋酸混合,醋酸的电离程度将 (填“增大”“不变”或“减小”)(水的浓度视为常数).
(5)用惰性电极电解0.1mol?L-1 D与0.1mol?L-1 C各100mL混合后的溶液,电解一段时间后,阴极质量 (填“增大”“不变”或“减小”,下同);溶液的pH .
(6)向(5)中所得溶液中加入足量铁粉,则所能溶解的铁粉质量为 g.
已知:
①A、B两溶液呈碱性,C、D、E溶液呈酸性.
②向E溶液中逐滴滴加B溶液至过量,沉淀量先增加后减少但不消失.
③D溶液与另外四种溶液反应都能产生沉淀.
请回答下列问题:
(1)写出A与D的化学式:A
(2)写出A与E溶液反应的离子方程式:
(3)已知:NaOH(aq)+HNO3(aq)═NaNO3(aq)+H2O(l)△H=-akJ?mol-1.请写出表示相同条件下B与C的稀溶液反应的中和热的热化学方程式:
(4)若25℃时,C、E及醋酸三种溶液的pH=4,则E和C溶液中由水电离出的c(H+)的比是
(5)用惰性电极电解0.1mol?L-1 D与0.1mol?L-1 C各100mL混合后的溶液,电解一段时间后,阴极质量
(6)向(5)中所得溶液中加入足量铁粉,则所能溶解的铁粉质量为
考点:物质的检验和鉴别的实验方案设计,电解原理
专题:物质检验鉴别题,离子反应专题
分析:由A、B溶液呈碱性,在所给的各种离子中,碳酸根水解显碱性,氢氧根有碱性,所以A、B中含有的阴离子为碳酸根和氢氧根,又因为铝离子和银离子水解显酸性,氢离子显酸性,所以C、D、E溶液含有的阳离子为H+、Al3+、Ag+,在所有的阳离子和阴离子组成的物质中,只有硫酸铝和氢氧化钡反应沉淀量先增加后减少但不消失,所以E是硫酸铝,B是氢氧化钡;
在所有的阳离子和阴离子组成的物质中,硝酸银能和盐酸、碳酸钠、硫酸铝、氢氧化钡反应生成沉淀,所以D是硝酸银,A为碳酸钠、C是盐酸;
综上所述,A、B、C、D、E分别为:Na2CO3、Ba(OH)2、HCl、AgNO3、Al2(SO4)3,以此来解答.
在所有的阳离子和阴离子组成的物质中,硝酸银能和盐酸、碳酸钠、硫酸铝、氢氧化钡反应生成沉淀,所以D是硝酸银,A为碳酸钠、C是盐酸;
综上所述,A、B、C、D、E分别为:Na2CO3、Ba(OH)2、HCl、AgNO3、Al2(SO4)3,以此来解答.
解答:
解:由A、B溶液呈碱性,在所给的各种离子中,碳酸根水解显碱性,氢氧根有碱性,所以A、B中含有的阴离子为碳酸根和氢氧根,又因为铝离子和银离子水解显酸性,氢离子显酸性,所以C、D、E溶液含有的阳离子为H+、Al3+、Ag+,在所有的阳离子和阴离子组成的物质中,只有硫酸铝和氢氧化钡反应沉淀量先增加后减少但不消失,所以E是硫酸铝,B是氢氧化钡;
在所有的阳离子和阴离子组成的物质中,硝酸银能和盐酸、碳酸钠、硫酸铝、氢氧化钡反应生成沉淀,所以D是硝酸银,A为碳酸钠、C是盐酸;
综上所述,A、B、C、D、E分别为:Na2CO3、Ba(OH)2、HCl、AgNO3、Al2(SO4)3,
(1)由上述分析可知,A为Na2CO3,D为AgNO3,故答案为:Na2CO3;AgNO3;
(2)A、E发生相互促进水解反应,离子反应为2Al3++3CO32-+3H2O═3CO2↑+2Al(OH)3↓,故答案为:2Al3++3CO32-+3H2O═3CO2↑+2Al(OH)3↓;
(3)NaOH(aq)+HNO3(aq)═NaNO3(aq)+H2O(l)△H=-akJ?mol-1.则B与C的稀溶液反应的中和热的热化学方程式为
Ba(OH)2(aq)+HCl(aq)═
BaCl2(aq)+H2O(l)△H=-akJ?mol-1,故答案为:
Ba(OH)2(aq)+HCl(aq)═
BaCl2(aq)+H2O(l)△H=-akJ?mol-1;
(4)盐酸溶液的pH=4,则c(H+)=10-4 mol/L,则c(OH-)=10-10 mol/L,OH-完全是由水电离产生,所以水电离出的氢离子浓度=10-10 mol/L;硫酸铝在溶液中水水解使水显示酸性,溶液中的氢离子浓度就是水电离出的氢离子浓度,pH=4,则c(H+)=10-4 mol/L,所以E和C溶液中由水电离出的c(H+)的比是106:1;C与醋酸混合,盐酸电离的氢离子抑制醋酸电离,醋酸的电离程度将减小,
故答案为:106:1;减小;
(5)用惰性电极电解0.1mol?L-1 AgNO3与0.1mol?L-1 HCl各100mL混合后的溶液,生成AgCl和硝酸,实质电解水,电解一段时间后,阴极质量不变,氢离子浓度增大,pH减小,故答案为:不变;减小;
(6)向(5)中所得溶液中加入足量铁粉,生成亚铁离子时溶解的Fe最多,则0.01mol硝酸则所能溶解的铁粉质量为0.01mol×
×56g/mol=0.21g,故答案为:0.21.
在所有的阳离子和阴离子组成的物质中,硝酸银能和盐酸、碳酸钠、硫酸铝、氢氧化钡反应生成沉淀,所以D是硝酸银,A为碳酸钠、C是盐酸;
综上所述,A、B、C、D、E分别为:Na2CO3、Ba(OH)2、HCl、AgNO3、Al2(SO4)3,
(1)由上述分析可知,A为Na2CO3,D为AgNO3,故答案为:Na2CO3;AgNO3;
(2)A、E发生相互促进水解反应,离子反应为2Al3++3CO32-+3H2O═3CO2↑+2Al(OH)3↓,故答案为:2Al3++3CO32-+3H2O═3CO2↑+2Al(OH)3↓;
(3)NaOH(aq)+HNO3(aq)═NaNO3(aq)+H2O(l)△H=-akJ?mol-1.则B与C的稀溶液反应的中和热的热化学方程式为
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
(4)盐酸溶液的pH=4,则c(H+)=10-4 mol/L,则c(OH-)=10-10 mol/L,OH-完全是由水电离产生,所以水电离出的氢离子浓度=10-10 mol/L;硫酸铝在溶液中水水解使水显示酸性,溶液中的氢离子浓度就是水电离出的氢离子浓度,pH=4,则c(H+)=10-4 mol/L,所以E和C溶液中由水电离出的c(H+)的比是106:1;C与醋酸混合,盐酸电离的氢离子抑制醋酸电离,醋酸的电离程度将减小,
故答案为:106:1;减小;
(5)用惰性电极电解0.1mol?L-1 AgNO3与0.1mol?L-1 HCl各100mL混合后的溶液,生成AgCl和硝酸,实质电解水,电解一段时间后,阴极质量不变,氢离子浓度增大,pH减小,故答案为:不变;减小;
(6)向(5)中所得溶液中加入足量铁粉,生成亚铁离子时溶解的Fe最多,则0.01mol硝酸则所能溶解的铁粉质量为0.01mol×
| 3 |
| 8 |
点评:本题考查离子的推断和无机物的推断,为高频考点,把握离子之间的反应、盐类水解等推断物质为解答的关键,侧重化学反应原理的考查,综合性较强,题目难度中等.

练习册系列答案
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案
相关题目
下列说法或解释不正确的是( )
| A、等物质的量浓度的下列溶液中,①NH4Al(SO4)2②NH4Cl③CH3COONH4④NH3?H2O,c(NH4+)由大到小的顺序是:②>①>④>③ |
| B、室温下,向0.01mol?L-1NH4HSO4溶液中滴加NaOH溶液至中性:c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+) |
| C、向0.2mol?L-1NaHCO3溶液中加如等体积0.1mol?L-1NaOH溶液:c(CO32-)>c(HCO3-)>c(OH-)>c(H+) |
| D、对于反应N2H4(l)=N2(g)+2H2(g)△H=-50.6kJ?mol-1在任何温度下都能自发进行 |
在如图装置中,a为Fe,b为碳棒,关于此装置的各种叙述正确的是( )


| A、a电极上有气体放出,b电极上无气泡,溶液pH变大 |
| B、a是正极,b是负极 |
| C、导线中有电子流动,外电路中,电子从a极到b极 |
| D、a极上发生了还原反应 |
设NA为阿伏加德罗常数,下列说法中不正确的是( )
| A、2.3g金属钠变为钠离子时失去的电子数是0.1NA |
| B、0.5NA个氯分子所占体积约为11.2L |
| C、28g氮气所含原子数为2NA |
| D、18g水所含的质子总数为10NA |
 甲酸为一元弱酸,在15mL 0.1mol/L KOH溶液中逐滴加入0.2mol/L甲酸溶液,溶液的pH变化和所加入的甲酸的体积关系描绘成如图所示曲线.下面有关微粒浓度的大小关系正确的是( )
甲酸为一元弱酸,在15mL 0.1mol/L KOH溶液中逐滴加入0.2mol/L甲酸溶液,溶液的pH变化和所加入的甲酸的体积关系描绘成如图所示曲线.下面有关微粒浓度的大小关系正确的是( )| A、在A、B间的任意一点上都存在:c(K+)>c(HCOO-)>c(OH-)>c(H+) |
| B、在B点:c(K+)=c(HCOO-)>c(OH-)=c(H+),且a=7.5 |
| C、在C点:c(HCOO-)>c(K+)>(H+)>c(OH-) |
| D、在D点:c(HCOO-)+c(HCOOH)=2c(K+) |
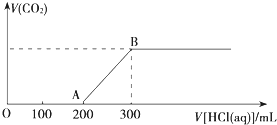 向100mL 3mol?L-1的NaOH溶液中缓慢通入一定量的CO2,充分反应,测得最后溶液的pH>7.
向100mL 3mol?L-1的NaOH溶液中缓慢通入一定量的CO2,充分反应,测得最后溶液的pH>7.