题目内容
7.某种H2和CO的混合气体,其密度是N2的一半,则氢气的体积百分含量约为( )| A. | 40% | B. | 46% | C. | 54% | D. | 63% |
分析 由ρ=$\frac{M}{{V}_{m}}$可知,摩尔质量与密度呈正比,其密度是氮气的一半,则混合气体的平均摩尔质量为14g/mol,可列方程式解答该题.
解答 解:混合气体的密度是氮气的一半,由ρ=$\frac{M}{{V}_{m}}$可知混合气体的平均摩尔质量为28g/mol×$\frac{1}{2}$=14g/mol,
设混合气体中含有xmol H2,ymolCO,则$\frac{2x+28y}{x+y}$=14,
整理可得x:y=7:6,
则氢气的体积百分含量为:$\frac{7}{7+6}$×100%≈54%,
故选C.
点评 本题考查物质的量的计算,题目难度不大,侧重于学生的计算能力的考查,为考试高频考点,注意把握气体的密度与摩尔质量的关系.

练习册系列答案
相关题目
17.已知某溶液中c(Na+)=0.2mol/L,c(Mg2+)=0.25mol/L,c(Cl-)=0.4mol/L,如果溶液中还有SO42-,那么c(SO42-)应为( )
| A. | 0.1 mol/L | B. | 0.3 mol/L | C. | 0.15 mol/L | D. | 0.5 mol/L |
15.下列说法不正确的是( )
| A. | Cl2、Br2、I2的分子间作用力依次减小 | |
| B. | 石英是由硅原子和氧原子构成的原子晶体,加热熔化时需破坏共价键 | |
| C. | 氢氧化钠在熔融状态下离子键被削弱,形成自由移动的离子,具有导电性 | |
| D. | 水电解生成氢气和氧气,有化学键的断裂和形成 |
2.气态烃1体积可与2体积氯化氢发生加成,生成氯代烷烃,此氯代烷烃1mol可与6mol氯气发生完全的取代反应,则该烃的结构简式为( )
| A. | CH2=CH2 | B. | CH2=CHCH=CH2 | C. | CH4 | D. | CH≡C-CH3 |
12.下列物质中,属于酚类的是( )
| A. | 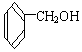 | B. | 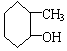 | C. | 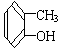 | D. | 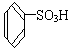 |
19.在下列给定条件的溶液中,一定能大量共存的离子组是( )
| A. | FeCl2溶液:K+、Na+、SO42-、AlO2- | |
| B. | 使紫色石蕊试液变红的溶液:Na+、Fe2+、NO3-、SO42- | |
| C. | 向存在大量Na+、Cl-的溶液中通入足量的NH3后:NH4+、Fe3+、SO42- | |
| D. | 在强酸性溶液中:K+、Fe2+、SO42-、Br- |
16.下列说法正确的是( )
| A. | 催化剂对反应热和反应的活化能均无影响 | |
| B. | 中和热△H=-57.3kJ/mol,则0.1mol稀硫酸与足量的氢氧化钡溶液反应放热11.46kJ | |
| C. | 放热反应在常温下一定很容易发生 | |
| D. | 破坏生成物化学键所需总能量小于破坏反应物化学键所需总能量的反应是吸热反应 |
8.下列物质的溶液在蒸发皿中加热蒸干并灼烧,最后得到该物质固体的是( )
| A. | 氯化铝 | B. | 碳酸氢钠 | C. | 硫酸镁 | D. | 高锰酸钾 |