��Ŀ����
�������������й㷺��Ӧ�ã�ij����������Ϊ��Ҫԭ���������ᡣ
��֪����550��ʱ��![]()
![]()
��һ���¶��£��������ڿ��������տ��ܷ������з�Ӧ(�������![]() ��
��![]() �����
�����
��Ϊ4��1)��![]() ,
,![]()
(1) 550��ʱ��6��4 g ![]() ������
������![]() ��ַ�Ӧ����
��ַ�Ӧ����![]() ���ų�����
���ų�����
9��83 kJ
(����ڡ��������ڡ���С�ڡ�)o
(2)��ʹ��Ӧ�ٵ�ƽ��������Ӧ�����ƶ������д�ʩ���е��� ��(����ĸ)
a����ƽ�������г���![]() b����ƽ�������г���
b����ƽ�������г���![]()
c���ı䷴Ӧ�Ĵ��� d�����ͷ�Ӧ���¶�
(3)Ϊʹ![]() ��ȫ����
��ȫ����![]() ������ʱҪʹ�ù�����
������ʱҪʹ�ù�����
 ��������������50��ʱ������¯����
��������������50��ʱ������¯����![]() ��
��
��������Ƕ���?
(4)720 g������![]() �ڿ�������ȫ���գ����ù���
�ڿ�������ȫ���գ����ù���
��![]() ��
��![]() �����ʵ���֮��n(
�����ʵ���֮��n(![]() )��n(
)��n(![]() )=6:
)=6: ![]() ��
��
��ʱ���Ŀ���Ϊ![]() mol��
mol��
����д������ڵĹ�ϵʽ�� ��
��������ͼ�л���![]() ��
��![]() �Ĺ�ϵ���ߡ�
�Ĺ�ϵ���ߡ�
��1���� ��2��bd
��3����FeS2Ϊ1 mol����ȫ������Ҫ��n(O2) = 2.75 mol������n(SO2) = 2 mol��
��������50%�����������2.75 �� 0.2 �� 1.5 = 20.625 mol��
SO2 ���������2 �� ( 20.625 + 2�� 2.75) = 10.0%
��4���� b = 2.5a + 60
�� �˵�Ϊ��8��80������9��82.5��֮���һ���߶�

 �����Ļ���������人������ϵ�д�
�����Ļ���������人������ϵ�д� ���������ּ���ÿһ��ȫ�º�����ҵ��ϵ�д�
���������ּ���ÿһ��ȫ�º�����ҵ��ϵ�д� ��ٽ������½������������ϵ�д�
��ٽ������½������������ϵ�д�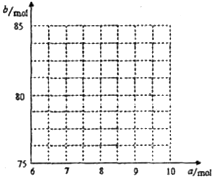
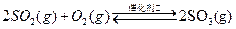
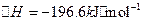
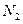 ��
��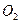 �����
�����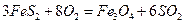 ,
,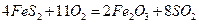
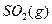 ������
������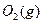 ��ַ�Ӧ����
��ַ�Ӧ����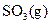 ���ų�����
���ų����� 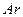 b����ƽ�������г���
b����ƽ�������г��� ��ȫ����
��ȫ����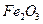 ������ʱҪʹ�ù�����
������ʱҪʹ�ù�����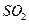 ��
��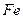 ��
�� �����ʵ���֮��n(
�����ʵ���֮��n( ��
�� mol��
mol��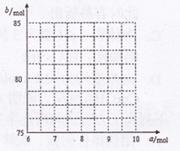
 ��������������50��ʱ������¯����
��������������50��ʱ������¯����