题目内容
17. 固体氧化物燃料电池是由美国西屋(Westinghouse)公司研制开发的.它以固体氧化锆一氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过.该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应.下列判断正确的是( )
固体氧化物燃料电池是由美国西屋(Westinghouse)公司研制开发的.它以固体氧化锆一氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过.该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应.下列判断正确的是( )| A. | 该电池的总反应方程式为:2H2+O2=2H2O | |
| B. | 电子由a极流向b极 | |
| C. | a极对应的电极反应式为2H2O+O2-4e=4OH- | |
| D. | 有O2参加反应的a极为电池的阳极 |
分析 该电池属于固体燃料电池,以固体氧化锆-氧化钇为电解质,电池工作时,正极上氧气得电子生成阳离子,则正极上反应为O2+4e-=2O2-;负极为氢气失电子发生氧化反应,负极:2H2-4e-+2O2-═2H2O,总反应为:2H2+O2=2H2O.
解答 解:A、该电池正极上反应为O2+4e-=2O2-,负极:2H2-4e-+2O2-═2H2O,总反应为:2H2+O2=2H2O,故A正确;
B、电子由负极b极流向正极a极,故B错误;
C、a极为正极,电极反应为:O2+4e-=2O2-,故C错误;
D、在燃料电池中,有O2参加的a极为原电池的正极,故D错误.
故选A.
点评 本题考查原电池的工作原理,涉及正负极的判断,电极反应式的书写等问题,题目难度不大,注意基础知识的积累.

练习册系列答案
相关题目
4.下列装置或操作正确并能达到实验目的( )
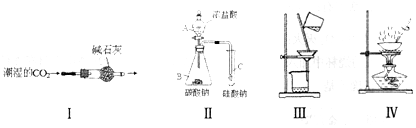

| A. | 用Ⅰ图装置,可得到干燥的CO2 | |
| B. | 用Ⅱ图装置,若C中出现白色沉淀,则可说明H2CO3的酸性强于H2SiO3 | |
| C. | 用Ⅲ图装置,可除去氯化钠溶液中的泥沙 | |
| D. | 用Ⅳ图装置,分离乙醇和水 |
5.实验室可以用来直接加热的玻璃仪器是( )
| A. | 小试管 | B. | 容量瓶 | C. | 量筒 | D. | 蒸发皿 |
2.《中国能源矿产地质调查报告》显示我国天然气水合物超千亿吨油当量.天然气主要成分为( )
| A. | H2 | B. | CO | C. | CH4 | D. | C2H4 |
9.既可用排水法又可用向上排空气法收集的气体是( )
| A. | NO | B. | O2 | C. | NH3 | D. | NO2 |
6.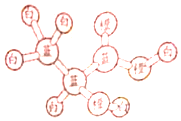 某有机物分子的球棍模型如图所示,图中“棍”代表化学键,不同颜色的“球”代表不同元素的原子,下列说法错误的是( )
某有机物分子的球棍模型如图所示,图中“棍”代表化学键,不同颜色的“球”代表不同元素的原子,下列说法错误的是( )
 某有机物分子的球棍模型如图所示,图中“棍”代表化学键,不同颜色的“球”代表不同元素的原子,下列说法错误的是( )
某有机物分子的球棍模型如图所示,图中“棍”代表化学键,不同颜色的“球”代表不同元素的原子,下列说法错误的是( )| A. | 1mol该有机物可与2molNa反应,生成1mol气体 | |
| B. | 该有机物可以发生加聚反应 | |
| C. | 该有机物可以发生取代反应,氧化反应、酯化反应 | |
| D. | 该有机物可以生成分子式为C6H8O4的酯 |
7.“碳呼吸电池”是一种新型能源装置,其工作原理如图.下列说法正确的是( )

| A. | 该装置是将电能转变为化学能 | |
| B. | 正极的电极反应为:C2O42--2e-=2CO2 | |
| C. | 每得到1 mol草酸铝,电路中转移3 mol电子 | |
| D. | 利用该技术可捕捉大气中的CO2 |
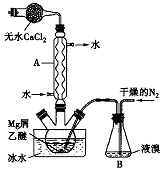 无水MgBr2可用作催化剂.实验室采用镁屑与液溴为原料制备无水MgBr2,装置如图所示(夹持仪器略去).主要步骤如下:
无水MgBr2可用作催化剂.实验室采用镁屑与液溴为原料制备无水MgBr2,装置如图所示(夹持仪器略去).主要步骤如下: A~H为中学化学中几种常见物质,它们之间的转化关系如图所示.常温下,A和G均为单质气体,同体C常用作干燥剂,E为无色、无味的液体,F为淡黄色粉末.回答下列问题:
A~H为中学化学中几种常见物质,它们之间的转化关系如图所示.常温下,A和G均为单质气体,同体C常用作干燥剂,E为无色、无味的液体,F为淡黄色粉末.回答下列问题: