题目内容
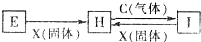 有关物质的转化关系如图所示(部分物质和条件已省去),C、X均是单质,H溶液呈浅绿色,I溶液呈棕黄色.下列有关判断正确的是( )
有关物质的转化关系如图所示(部分物质和条件已省去),C、X均是单质,H溶液呈浅绿色,I溶液呈棕黄色.下列有关判断正确的是( )| A、X固体可能是碘单质 |
| B、图中所示反应均为氧化还原反应 |
| C、1mol C与E溶液完全反应转移电子数为NA(NA为阿伏加德罗常数) |
| D、E、H、I溶液配制时,均需加酸防止其水解 |
考点:无机物的推断
专题:推断题
分析:H溶液呈浅绿色,I溶液呈棕黄色,可知H含有Fe2+,I含有Fe3+,C氧化性气体,氧化性应大于Fe3+,一般为氯气,X为还原性固体,应为Fe,E能与Fe反应生成Fe2+,可为非氧化性酸等,以此解答该题.
解答:
解:A.H溶液呈浅绿色含Fe2+,I溶液呈棕黄色含Fe3+,X固体为还原剂,而碘单质无法将Fe3+还原为Fe2+,故A错误;
B.图中所示H、I溶液的转化反应为氧化还原反应,E转化为H需加还原剂X,也是氧化还原反应,都存在Fe元素化合价的变化,故B正确;
C.气体为强氧化性气体,1mol C与H溶液完全反应转移电子数不一定为NA,若为氯气则为2NA,故C错误;
D.E可能为稀的强酸溶液如盐酸,则无需防止其水解,故D错误.
故选B.
B.图中所示H、I溶液的转化反应为氧化还原反应,E转化为H需加还原剂X,也是氧化还原反应,都存在Fe元素化合价的变化,故B正确;
C.气体为强氧化性气体,1mol C与H溶液完全反应转移电子数不一定为NA,若为氯气则为2NA,故C错误;
D.E可能为稀的强酸溶液如盐酸,则无需防止其水解,故D错误.
故选B.
点评:本题考查无机物的推断,为高频考点,侧重于学生的分析能力的考查,注意把握物质的颜色,为解答该题的关键,结合物质的性质以及氧化还原反应的特点解答,难度中等.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
下列各项叙述正确的是( )
| A、清晨,在树林中,常看到从枝叶间透过的一道道光柱,这是胶体产生的丁达尔效应 |
| B、某固体A能导电,一定是金属 |
| C、由同种元素组成的物质肯定属于纯净物 |
| D、由氯化铵溶液呈弱酸性可知氯化铵是弱电解质 |
如图所示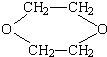 是一种常见的溶剂,是它可以通过下列路线制得:
是一种常见的溶剂,是它可以通过下列路线制得:
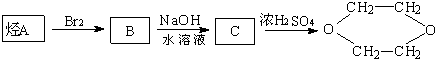
则A可能是( )
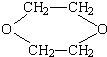 是一种常见的溶剂,是它可以通过下列路线制得:
是一种常见的溶剂,是它可以通过下列路线制得:
则A可能是( )
| A、乙烯 | B、乙醇 | C、乙二醇 | D、乙醚 |
据《自然》杂志网站2013年1月3日报道,德国物理学家用钾原子首次造出一种低于绝对零度的量子气体.科学家称这一成果为“实验的绝技”,为将来造出负温度物质、新型量子设备打开了大门,有助于揭开宇宙中的许多奥密.钾的化合物在科技、生活生产中应用广泛,则下列叙述正确的是( )
| A、超氧化钾(KO2)可作为飞船、潜艇等密闭系统的氧气再生剂,若有1molKO2被消耗,可产生O2 22.4L |
| B、高锰酸钾溶液是实验室常用的试剂,欲配置1.00L 0.10mol/L的KMnO4溶液,可将15.8g KMnO4溶于1L水中 |
| C、KNO3可用于制造黑火药,已知黑火药反应为S+2KNO3+3C=K2S+N2↑+3CO2↑,若有1mol KNO3被消耗,则该反应转移电子5×6.02×1023 |
| D、氰化钾(KCN、剧毒)可用于电镀,使镀层更细致,65g KCN晶体中,离子总数为2×6.02×1023 |
在由硫酸钾、硫酸铁和硫酸组成的混合溶液中,C(H+)=0.1mol/L,C(Fe3+)=0.3mol/L,C(SO42-)=0.6mol/L,则C(K+)为( )
| A、0.1mol/L |
| B、0.2mol/L |
| C、0.3mol/L |
| D、0.4mol/L |
决定物质体积大小的主要因素,其中不包括( )
| A、微粒间引力 |
| B、微粒的数目 |
| C、微粒的大小 |
| D、微粒间平均距离 |
当温度达到374℃,压强为2.2×104KPa时,水处于超临界状态,此时水具有较高浓度的H+和OH-,能溶解更多的有机物质,下列对临界状态水的推测正确的是( )
| A、超临界水的pH较常温时升高 |
| B、超临界水的离子积增大 |
| C、超临界水发生了化学变化 |
| D、大多数有机物在超临界水中溶解度更小 |