题目内容
据《自然》杂志网站2013年1月3日报道,德国物理学家用钾原子首次造出一种低于绝对零度的量子气体.科学家称这一成果为“实验的绝技”,为将来造出负温度物质、新型量子设备打开了大门,有助于揭开宇宙中的许多奥密.钾的化合物在科技、生活生产中应用广泛,则下列叙述正确的是( )
| A、超氧化钾(KO2)可作为飞船、潜艇等密闭系统的氧气再生剂,若有1molKO2被消耗,可产生O2 22.4L |
| B、高锰酸钾溶液是实验室常用的试剂,欲配置1.00L 0.10mol/L的KMnO4溶液,可将15.8g KMnO4溶于1L水中 |
| C、KNO3可用于制造黑火药,已知黑火药反应为S+2KNO3+3C=K2S+N2↑+3CO2↑,若有1mol KNO3被消耗,则该反应转移电子5×6.02×1023 |
| D、氰化钾(KCN、剧毒)可用于电镀,使镀层更细致,65g KCN晶体中,离子总数为2×6.02×1023 |
考点:氧化还原反应的计算,物质的量的相关计算,物质的量浓度的相关计算
专题:
分析:A.结合反应的方程式4KO2+2CO2=2K2CO3+3O2以及气体存在的条件判断;
B.水的体积不等于溶液的体积;
C.该反应中,硫元素化合价由0价变为-2价,N元素化合价由+5价变为0价,碳元素化合价由0价变为+4价,结合化合价的变化计算;
D.65g KCN为1mol,含有的离子分别为K+、CN-.
B.水的体积不等于溶液的体积;
C.该反应中,硫元素化合价由0价变为-2价,N元素化合价由+5价变为0价,碳元素化合价由0价变为+4价,结合化合价的变化计算;
D.65g KCN为1mol,含有的离子分别为K+、CN-.
解答:
解:A.反应的方程式为4KO2+2CO2=2K2CO3+3O2,若有1molKO2被消耗,可产生O2 0.75mol,由于气体存在的条件未知,则不能确定体积,故A错误;
B.15.8g KMnO4为0.1mol,水的体积不等于溶液的体积,故B错误;
C.该反应中,硫元素化合价由0价变为-2价,N元素化合价由+5价变为0价,碳元素化合价由0价变为+4价,有1mol KNO3被消耗,则消耗1.5molC,失去6mol电子,故C错误;
D.65g KCN为1mol,含有的离子分别为K+、CN-,离子总数为2×6.02×1023,故D正确.
故选D.
B.15.8g KMnO4为0.1mol,水的体积不等于溶液的体积,故B错误;
C.该反应中,硫元素化合价由0价变为-2价,N元素化合价由+5价变为0价,碳元素化合价由0价变为+4价,有1mol KNO3被消耗,则消耗1.5molC,失去6mol电子,故C错误;
D.65g KCN为1mol,含有的离子分别为K+、CN-,离子总数为2×6.02×1023,故D正确.
故选D.
点评:本题考查氧化还原反应的计算,为高频考点,侧重于学生的分析能力和计算能力的考查,注意把握元素化合价的变化,为解答该题的关键,难度中等.

练习册系列答案
相关题目
2006年5月15日,国家食品药品监督管理局通报查处了齐齐哈尔第二制药有限公司使用工业溶剂二甘醇(HO-CH2-CH2-O-CH2-CH2-OH)代替药用溶剂丙二醇(HO-CH2-CH2-CH2-OH)的事件.最新统计,目前确定齐齐哈尔第二制药有限公司生产的“亮菌甲素”假药造成的死亡人数已有9人.下列关于二甘醇说法正确的是( )
| A、二甘醇和丙二醇性质完全相同 |
| B、二甘醇和丙二醇互为同系物 |
| C、二甘醇沸点可能比丙二醇高 |
| D、二甘醇在人体中的降解产物草酸(HOOC-COOH)对人体有害 |
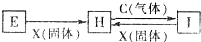 有关物质的转化关系如图所示(部分物质和条件已省去),C、X均是单质,H溶液呈浅绿色,I溶液呈棕黄色.下列有关判断正确的是( )
有关物质的转化关系如图所示(部分物质和条件已省去),C、X均是单质,H溶液呈浅绿色,I溶液呈棕黄色.下列有关判断正确的是( )| A、X固体可能是碘单质 |
| B、图中所示反应均为氧化还原反应 |
| C、1mol C与E溶液完全反应转移电子数为NA(NA为阿伏加德罗常数) |
| D、E、H、I溶液配制时,均需加酸防止其水解 |
下列反应的离子方程式正确的是( )
| A、铁和稀盐酸反应 2Fe+6H+=2Fe3++3H2↑ |
| B、碳酸钙溶于稀盐酸中 CO32-+2H+=CO2↑+H2O |
| C、碳酸氢钠溶液与盐酸反应 HCO3-+H+=CO2↑+H2O |
| D、氧化铜与盐酸反应 O2-+2H+=H2O |
下列有关物质的表达式正确的是( )
| A、乙酸乙酯的结构简式:CH3CH2COOCH3 |
B、2-甲基-2-戊烯的键线式: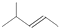 |
| C、乙醇的结构简式:CH3CH2OH |
| D、1,3-丁二烯的分子式:C4H8 |