题目内容
17.对于反应:N2(g)+3H2(g)?2NH3(g)△H<0,下列图象不正确的是( )| A. | 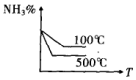 | B. | 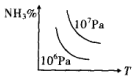 | C. | 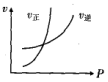 | D. | 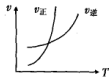 |
分析 合成氨为气体体积减小、放热的反应,升高温度反应速率加快,平衡逆向移动;增大压强,反应速率加快,平衡正向移动,以此来解答.
解答 解:A.升高温度反应速率加快,平衡逆向移动,则温度高的先达到平衡,且生成物的含量低,与图象一致,故A正确;
B.温度高时氨气的含量低,且相同温度下,压强越大,平衡时氨气的含量越大,与图象一致,故B正确;
C.由交叉点后增大压强,平衡正向移动,正反应速率大于逆反应速率,与图象一致,故C正确;
D.升高温度,平衡逆向移动,则逆反应速率大于正反应速率,与图不符,故D错误;
故选D.
点评 本题考查化学平衡的移动,为高频考点,把握温度、压强对平衡移动的影响为解答的关键,侧重分析与应用能力的考查,注意反应的特点及平衡移动原理的应用,题目难度不大.

练习册系列答案
相关题目
8.将含有Fe2O3、SiO2杂质的Al2O3样品提纯,其流程示意图如图:下列说法错误的是( )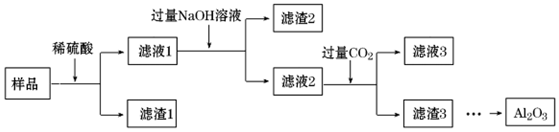

| A. | 滤渣1 的主要成分为SiO2 | |
| B. | 可用KSCN溶液检验滤液1中的Fe 3+ | |
| C. | 滤液2为纯净的Na AlO2溶液 | |
| D. | 将滤渣3 洗涤、干燥、灼烧,可以得到Al2O3 |
8.常温下,往H2O2溶液中滴加少量FeSO4溶液,可发生如下两个反应:2Fe2++H2O2+2H+→2Fe3++2H2O①2Fe3++H2O2→2Fe2++O2↑+2H+②下列说法错误的是( )
| A. | 由方程式①可知,H2O2的氧化性比Fe3+强 | |
| B. | 在H2O2分解过程中,溶液的H+的物质的量逐渐上升 | |
| C. | 在H2O2分解过程中,Fe2+和Fe3+的总量保持不变 | |
| D. | H2O2生产过程要严格避免混入Fe2+ |
5.往水中加入下列物质,对水的电离平衡不产生影响的是( )
| A. | NaHSO4 | B. | CH3COOK | C. | KAl(SO4)2 | D. | NaI |
12.下列物质分类正确的是( )
| A. | SO2、SiO2、CO2均为酸性氧化物 | B. | 稀豆浆、氯化铁溶液均为胶体 | ||
| C. | 烧碱、四氯化碳、氨气均为电解质 | D. | 氯水、漂白粉、小苏打均为纯净物 |
9.物质间的转化关系中不能全部通过一步反应完成的是( )
| A. | Na→NaOH→Na2CO3→NaCl | B. | Mg→MgCl2→Mg(OH)2→MgO | ||
| C. | Al→Al2O3→Al(OH)3→AlCl3 | D. | Cl2→Ca(ClO)2→HClO→HCl |
6.在给定的条件下,下列选项所示的物质间转化均能实现的是( )
| A. | Fe$→_{高温}^{Al_{2}O_{3}}$Al$\stackrel{NaOH(aq)}{→}$H2 | |
| B. | MgCl2•6H2O$→_{△}^{HCl}$MgCl2$\stackrel{熔融电解}{→}$Mg | |
| C. | NH3$→_{催化剂}^{O_{2}}$NO$\stackrel{NaOH(aq)}{→}$NaNO2 | |
| D. | SO2$\stackrel{BaCl_{2}(aq)}{→}$BaSO3(s)$\stackrel{O_{2}}{→}$BaSO4(s) |
6.下列叙述正确的是( )
| A. | 向氢氧化钠溶液中边滴加饱和FeCl3溶液边振荡制备Fe(OH)3胶体 | |
| B. | 分散系中分散质粒子直径由小到大的正确顺序是:溶液<胶体<浊液 | |
| C. | Fe(OH)3胶体的电泳现象证明此胶体带正电荷 | |
| D. | 胶体区别于其他分散系的根本原因是胶体有丁达尔效应 |
 .
.