题目内容
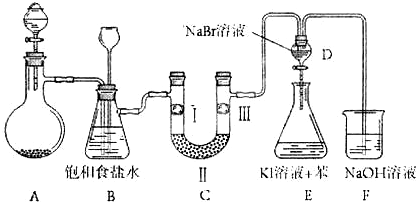
(10分)下图是实验室制备氯气并进行一系列相关实验的装置(夹持设备已略)。

(1)制备氯气选用的药品为:漂粉精固体和浓盐酸,相关的化学反应方程式为:
。
(2)装置B中饱和食盐水的作用是 ;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象 。
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中I、II、III依次放入 。
|
|
a |
b |
c |
d |
|
I |
干燥的有色布条 |
干燥的有色布条 |
湿润的有色布条 |
湿润的有色布条 |
|
II |
碱石灰 |
硅胶 |
浓硫酸 |
无水氯化钙 |
|
III |
湿润的有色布条 |
湿润的有色布条 |
干燥的有色布条 |
干燥的有色布条 |
(4)设计装置D、E的目的是比较氯、溴、碘的非金属性。当向D中缓缓通入足量氯气时,可以看到无色溶液逐渐变为深棕红色,说明氯的非金属性大于溴。打开活塞,将装置D中少量溶液加入装置E中,振荡。观察到的现象是 。该现象
(填“能”或“不能”)说明溴的非金属性强于碘,原因是 。
(1)Ca(ClO)2 + 4HCl(浓)=== CaCl2 + 2Cl2↑+ 2H2O(2分)
(2)除去Cl2中的HCl(1分) 锥形瓶中液面下降,长颈漏斗中液面上升(2分)
(3)d (1分)
(4)E中溶液分为两层,上层(苯层)为紫红色(2分)
不能(1分) 过量的Cl2也可将I-氧化为I2(1分)
【解析】(1)漂粉精固体和浓盐酸反应生成氯气,反应的化学方程式是Ca(ClO)2 + 4HCl(浓)=== CaCl2 + 2Cl2↑+ 2H2O。
(2)由于浓盐酸易挥发,所以生成的氯气中混有氯化氢,所以饱和食盐水的作用是除去Cl2中的HCl气体;如果后面导管发生堵塞,则B中压强会增大,依次锥形瓶中液面下降,长颈漏斗中液面上升,据此可以判断是否堵塞。
(3)由于氯气能和水反应生成次氯酸,而次氯酸具有漂白性。所以在Ⅱ处应该放置固体干燥剂。而在I、Ⅲ处则是布条,起对照的作用,因此正确的答案选d。
(4)由于生成的溴能把碘化钾氧化生成单质碘,而碘易溶在有机溶剂中,所以实验现象是E中溶液分为两层,上层(苯层)为紫红色。但由于氯气是过量的,而过量的Cl2也可将I-氧化为I2,所以不能数目溴的非金属性强于碘的。

下图是实验室制备氯气并进行一系列相关实验的装置(夹持设备已略)。
(1)制备氯气选用的药品为:漂白粉固体和浓盐酸,相关的化学反应方程式为:___________________________________。
(2)装置B中饱和食盐水的作用是_______;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象______________________________。
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入__________。
| | a | b | c | d |
| Ⅰ | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
| Ⅱ | 碱石灰 | 硅胶 | 浓硫酸 | 无水氯化钙 |
| Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
(5)打开活塞,将装置D中少量溶液加入装置E中,振荡。观察到的现象是__________。
(6)装置F的作用是__________,有人提出,F中的药品可改用足量的NaHSO
 溶液,判断改用NaHSO
溶液,判断改用NaHSO 溶液是否可行__________(填“是”或“否”)。如果答“否”,用离子方程式解释原因____________________(答“是”则不用解释)。
溶液是否可行__________(填“是”或“否”)。如果答“否”,用离子方程式解释原因____________________(答“是”则不用解释)。