题目内容
9.下列反应的离子方程式正确的是( )| A. | 硫化亚铁中加入稀硫酸 2H++S2-→H2S↑ | |
| B. | 向苯酚钠溶液中通入少量的CO2 -O-+CO2+H2O→ -O-+CO2+H2O→ -OH+HCO3- -OH+HCO3- | |
| C. | 向碳酸氢钠溶液中滴入少量石灰水 HCO3-+Ca2++OH-→CaCO3↓+H2O | |
| D. | 向明矾溶液中加入过量的氨水 A13++3NH3•H2O→Al(OH)3↓+3NH4+ |
分析 A.硫化亚铁是难溶物质,要保留化学式;
B.反应生成苯酚和碳酸氢钠;
C.向碳酸氢钠溶液中滴入少量石灰水生成碳酸钙、碳酸钠和水;
D.铝离子与NH3•H2O反应生成氢氧化铝沉淀和铵根离子.
解答 A.硫化亚铁是难溶物质,要保留化学式,硫化亚铁中加入稀硫酸的离子方程式为:2H++FeS=Fe2++H2S↑,故A错误;
B.向苯酚钠溶液中通入少量的CO2反应生成苯酚和碳酸氢钠,反应的离子方程式为: -O-+CO2+H2O→
-O-+CO2+H2O→ -OH+HCO3-,故B正确;
-OH+HCO3-,故B正确;
C.向碳酸氢钠溶液中滴入少量石灰水生成碳酸钙、碳酸钠和水,反应的离子方程式为:2HCO3-+Ca2++2OH-=CaCO3↓+CO32-+2H2O,故C错误;
D.铝离子与NH3•H2O反应生成氢氧化铝沉淀和铵根离子,反应的离子方程式为:A13++3NH3•H2O=Al(OH)3↓+3NH4+,故D正确.
故选BD.
点评 本题考查了离子反应方程式正误判断,明确物质的性质、离子反应先后顺序、酸性强弱、盐类水解等知识点即可解答,题目难度不大.

练习册系列答案
相关题目
20. 某有机物结构式如图所示,其一氯代物共有(不考虑立体异构)( )
某有机物结构式如图所示,其一氯代物共有(不考虑立体异构)( )
 某有机物结构式如图所示,其一氯代物共有(不考虑立体异构)( )
某有机物结构式如图所示,其一氯代物共有(不考虑立体异构)( )| A. | 3种 | B. | 4种 | C. | 5种 | D. | 7种 |
17. 将不可再生的天然气、石油、煤等化石燃料转化利用、变废为宝已成为当务之急.
将不可再生的天然气、石油、煤等化石燃料转化利用、变废为宝已成为当务之急.
(1)根据键能数据估算CH4+4F2=CF4+4HF的反应热△H=-1940kJ•mol-1.
(2)甲醇、二甲醚(CH3OCH3)被称为21世纪的新型燃料,均可利用CO和H2反应合成.
①某燃料电池以二甲醚为原料,熔融碳酸盐为电解质,其负极反应如下:CH3OCH3+6CO${\;}_{3}^{2-}$-12e-=8CO2+3H2O.写出该燃料电池的正极反应式:O2+4e-+2CO2=2CO32-.
②废水中含甲醇对水质会造成污染,Co3+可将甲醇氧化为CO2.某同学以Pt作电极电解酸性含甲醇废水与CoSO4混合液模拟工业除污原理,其阳极反应式为Co2+-e-=Co3+.
(3)某企业采用如图所示原理处理化石燃料开采、加工过程产生的H2S废气.
①电解池中电极A、B均为惰性电极,其中A为电解池的B极;电极B所得到的物质X的分子式为H2.
②反应池中发生的离子反应方程式为H2S+2Fe3+=2Fe2++S↓+2H+.
 将不可再生的天然气、石油、煤等化石燃料转化利用、变废为宝已成为当务之急.
将不可再生的天然气、石油、煤等化石燃料转化利用、变废为宝已成为当务之急.(1)根据键能数据估算CH4+4F2=CF4+4HF的反应热△H=-1940kJ•mol-1.
| 化学键 | C-H | C-F | H-F | F-F |
| 键能/(kJ•mol-1) | 414 | 489 | 565 | 155 |
①某燃料电池以二甲醚为原料,熔融碳酸盐为电解质,其负极反应如下:CH3OCH3+6CO${\;}_{3}^{2-}$-12e-=8CO2+3H2O.写出该燃料电池的正极反应式:O2+4e-+2CO2=2CO32-.
②废水中含甲醇对水质会造成污染,Co3+可将甲醇氧化为CO2.某同学以Pt作电极电解酸性含甲醇废水与CoSO4混合液模拟工业除污原理,其阳极反应式为Co2+-e-=Co3+.
(3)某企业采用如图所示原理处理化石燃料开采、加工过程产生的H2S废气.
①电解池中电极A、B均为惰性电极,其中A为电解池的B极;电极B所得到的物质X的分子式为H2.
②反应池中发生的离子反应方程式为H2S+2Fe3+=2Fe2++S↓+2H+.
4.化合物FeO具有NaCl型结构.在天然样品中,往往由于部分Fe2+被Fe3+代替,晶体存在缺陷,使n(Fe):n(O)<1.用Fe2+和Fe3+可以将组成为Fe0.95O的某天然FeO样品表示为( )
| A. | Fe2+0.45Fe3+0.50O | B. | Fe2+0.85Fe 3+0.10O | ||
| C. | Fe2+0.15Fe3+0.80O | D. | Fe2+0.20Fe 3+0.75O |
14.某化合物的结构(键线式)及球棍模型如图1:该有机分子的核磁共振波谱图如图2(单位是ppm).下列关于该有机物的叙述正确的是( )
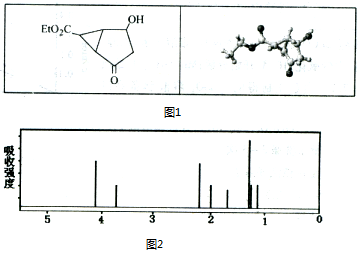

| A. | 该有机物不同化学环境的氢原子有8种 | |
| B. | 该有机物属于芳香族化合物 | |
| C. | 键线式中的Et代表的基团为-CH3 | |
| D. | 该有机物在一定条件下能够发生加成反应、取代反应,但不能发生消去反应 |
1.近年来美国研究人员合成了光伏电池新型硅材料--Si24(如图所示).下列相关说法正确的是( )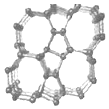

| A. | Si24是一种新型化合物 | |
| B. | Si24是硅的一种同素异形体 | |
| C. | Si24易与稀硫酸反应生成氢气 | |
| D. | 硅太阳能电池供电原理与原电池相同 |
18.某稀硫酸和稀硝酸的混合溶液中c(SO42-)+c(NO3-)=2.5mol•L-1,取200mL该混合酸,则能溶解铜的最大质量为( )
| A. | 12.8 g | B. | 19.2 g | C. | 32.0 g | D. | 38.4 g |
11. 某无色溶液,只可能含有以下离子中的若干种(忽略由水电离产生的H+、OH-):H+、NH4+、K+、Mg2+、Cu2+、Al3+,NO3-、CO32-、SO42-,现取三份100mL溶液进行如下实验:
某无色溶液,只可能含有以下离子中的若干种(忽略由水电离产生的H+、OH-):H+、NH4+、K+、Mg2+、Cu2+、Al3+,NO3-、CO32-、SO42-,现取三份100mL溶液进行如下实验:
①第一份加足量AgNO3溶液后,有白色沉淀产生.
②第二份加足量BaCl2溶液后,有白色沉淀产生,经洗涤、干燥后,沉淀质量为6.99g.
③第三份逐滴滴加NaOH溶液,测得沉淀与NaOH溶液的体积关系如图
根据上述实验,以下推测不正确的是( )
 某无色溶液,只可能含有以下离子中的若干种(忽略由水电离产生的H+、OH-):H+、NH4+、K+、Mg2+、Cu2+、Al3+,NO3-、CO32-、SO42-,现取三份100mL溶液进行如下实验:
某无色溶液,只可能含有以下离子中的若干种(忽略由水电离产生的H+、OH-):H+、NH4+、K+、Mg2+、Cu2+、Al3+,NO3-、CO32-、SO42-,现取三份100mL溶液进行如下实验:①第一份加足量AgNO3溶液后,有白色沉淀产生.
②第二份加足量BaCl2溶液后,有白色沉淀产生,经洗涤、干燥后,沉淀质量为6.99g.
③第三份逐滴滴加NaOH溶液,测得沉淀与NaOH溶液的体积关系如图
根据上述实验,以下推测不正确的是( )
| A. | 依据电荷守恒,原溶液中NO3-的物质的量应为0.03mol | |
| B. | 原溶液一定不存在H+、Cu2+、CO32- | |
| C. | 原溶液确定含Mg2+、Al3+、NH4+,且n(Mg2+):n(Al3+):n(NH4+)=1:1:2 | |
| D. | 实验所加的NaOH的浓度为2mol•L-1 |