题目内容
18.某稀硫酸和稀硝酸的混合溶液中c(SO42-)+c(NO3-)=2.5mol•L-1,取200mL该混合酸,则能溶解铜的最大质量为( )| A. | 12.8 g | B. | 19.2 g | C. | 32.0 g | D. | 38.4 g |
分析 反应的离子方程式为3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O,要使溶解铜的质量最大,则氢离子和硝酸根浓度满足化学计量数即4:1,硝酸全部起氧化剂作用,设硫酸浓度为x,则硝酸浓度为:2.5mol/L-x,溶液中氢离子浓度共:2x+(2.5mol/L-x),则$\frac{2x+(2.5mol/L-x)}{.5mol/L-x}$=4:1,解得x=1.5mol/L,硝酸浓度为1mol/L,根据方程式可计算溶解铜的质量.
解答 解:反应的离子方程式为:3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O,要使溶解铜的质量最大,则氢离子和硝酸根浓度满足化学计量数4:1,硝酸全部起氧化剂作用,
设硫酸浓度为x,则硝酸浓度为:2.5mol/L-x,溶液中氢离子浓度共:2x+(2.5mol/L-x),
则$\frac{2x+(2.5mol/L-x)}{.5mol/L-x}$=4:1,
解得:x=1.5mol/L,
则硝酸浓度为:2.5mol/L-x=1mol/L,硝酸得物质的量为:0.2L×1mol/L=0.2mol,
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
3×64g 2mol
m 0.2mol
则能溶解铜的最大质量为:m=$\frac{3×64g×0.2mol}{2mol}$=19.2g,
故选B.
点评 本题考查物质的量的计算、化学方程式的计算,题目难度中等,根据反应原理得出“氢离子和硝酸根浓度满足化学计量数4:1”为解答关键,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
8.下列各项化学用语表达正确的是( )
| A. | NaCl的电子式: | B. | 次氯酸的结构式:H-Cl-O | ||
| C. | CO2的分子模型示意图: | D. | O2-的离子结构示意图: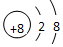 |
9.下列反应的离子方程式正确的是( )
| A. | 硫化亚铁中加入稀硫酸 2H++S2-→H2S↑ | |
| B. | 向苯酚钠溶液中通入少量的CO2 -O-+CO2+H2O→ -O-+CO2+H2O→ -OH+HCO3- -OH+HCO3- | |
| C. | 向碳酸氢钠溶液中滴入少量石灰水 HCO3-+Ca2++OH-→CaCO3↓+H2O | |
| D. | 向明矾溶液中加入过量的氨水 A13++3NH3•H2O→Al(OH)3↓+3NH4+ |
6.仪器名称为“蒸发皿”的是( )
| A. | 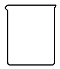 | B. | 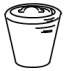 | C. | 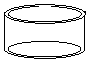 | D. |  |
3.下列说法正确的是( )
| A. | pH=3的醋酸和pH=11的NaOH溶液等体积混合后,pH>7 | |
| B. | 若物质的量浓度相同的NH4Cl和NH3•H2O混合溶液pH>7,则在pH=7的NH4Cl和NH3•H2O混合溶液中:c(NH4+)>c(NH3•H2O) | |
| C. | 0.1mol•L-1的NaHSO3溶液:c(H+)-c(OH-)=c(SO32-)-2c(H2SO3) | |
| D. | 0.1mol/LNa2CO3溶液和0.1mol/LNaHSO4溶液等体积混合,溶液中c(Na+)+c(H+)=c(CO32-)+c(SO42-)+c(HCO3-)+c(OH-) |
20.将某些化学知识用数轴表示,可以收到直观形象、简明易记的效果.用数轴表示的下列化学知识中正确的是( )
| A. | 分散系的分类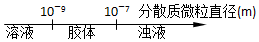 | |
| B. | Fe与Cl2反应的产物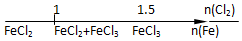 | |
| C. | 向AlCl3溶液滴加NaOH溶液后铝的存在形式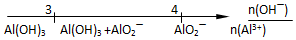 | |
| D. | Na与O2反应的产物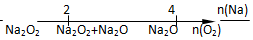 |
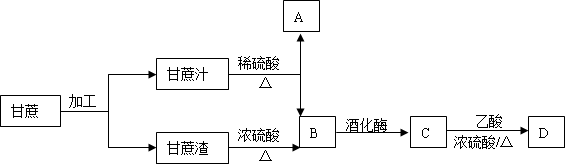
 .
.