题目内容
13.下列关于物质的性质、用途、制备或检验的叙述正确的是( )| A. | 使湿润的蓝色石蕊试纸变红的气体是氨气 | |
| B. | 瓷坩埚可用作Na2CO3与石英制Na2SiO3的反应容器 | |
| C. | 热Na2CO3溶液更利于清洗餐具上的油污 | |
| D. | 某溶液中加入BaCl2溶液,产生不溶于稀硝酸的沉淀,该溶液一定含有SO42- |
分析 A.检验氨气,利用红色石蕊试纸;
B.瓷坩埚中含二氧化硅与碳酸钠反应;
C.热的纯碱溶液水解,碱性增强,利用油污的水解;
D.沉淀可能为AgCl.
解答 解:A.检验氨气,利用红色石蕊试纸,则使湿润的红色石蕊试纸变蓝的气体是氨气,故A错误;
B.瓷坩埚中含二氧化硅与碳酸钠反应,则应选铁坩埚,故B错误;
C.热的纯碱溶液水解,碱性增强,利用油污的水解,则热Na2CO3溶液更利于清洗餐具上的油污,故C正确;
D.沉淀可能为AgCl,则不能检验是否含硫酸根离子,故D错误;
故选C.
点评 本题考查物质的性质、应用及检验,为高频考点,把握物质的性质、发生的反应及应用为解答的关键,侧重分析与应用能力的考查,综合性较强,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
1.现有四种有机物①C3H7Cl②C3H8O③C3H6O④C3H6O2,下列有关说法正确的是( )
| A. | ①、②、③、④均只有两种结构 | |
| B. | ①的同分异构体数目与④的相同 | |
| C. | ③一定是丙醛 | |
| D. | 若②与④能发生酯化反应,则生成的酯最多有2种 |
8.目前人们对环境保护、新能源开发很重视.
(1)汽车尾气中含有CO、NO2等有毒气体,对汽车加装尾气净化装置,可使有毒气体转化为无毒气体.4CO(g)+2NO2(g)?4CO2(g)+N2(g)△H=-1200 kJ•mol-1
对于该反应,温度不同(T2>T1)、其他条件相同时,下列图象正确的是乙(填代号).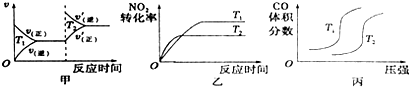
(2)用活性炭还原法也可以处理氮氧化物,某研究小组向某密闭容器加入一定量的活性炭和NO,发生反应C(s)+2NO(g)?N2(g)+CO2(g)△H在T1℃时,反应进行到不同时间测得各物质的量浓度如下:
①根据图表数据分析T1℃时,该反应在0~20min的平均反应速率v(CO2)=0.015 mol•L-1•min-1;计算该反应的平衡常数K=0.56.
②30min后,只改变某一条件,根据上表的数据判断改变的条件可能是bc(填字母代号).
a.加入一定量的活性炭 b.通入一定量的NO
c.适当缩小容器的体积 d.加入合适的催化剂
③若30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为5:3:3,则达到新平衡时NO的转化率 (填“升高”或“降低”),△H<0(填“>”或“<”).
(3)以CO2与NH3为原料可合成化肥尿素[化学式为CO(NH2)2].已知:
①2NH3(g)+CO2(g)=NH2CO2NH4(s)△H=-l59.5kJ/mol
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g)△H=+116.5kJ/mol
③H2O(l)=H2O(g)△H=+44.0kJ/mol
写出CO2与NH3合成尿素和液态水的热化学反应方程式2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(l)△H=-87.0 kJ•mol-1.
(4)一种氨燃料电池,使用的电解质溶液是2mol/L-1的KOH溶液.
电池反应为:4NH3+3O2=2N2+6H2O;
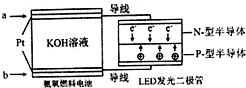
请写出通入a气体一极的电极反应式为2NH3+6OH--6e-=N2+6H2O;每消耗3.4g NH3转移电子的物质的量为0.6 mol.
(1)汽车尾气中含有CO、NO2等有毒气体,对汽车加装尾气净化装置,可使有毒气体转化为无毒气体.4CO(g)+2NO2(g)?4CO2(g)+N2(g)△H=-1200 kJ•mol-1
对于该反应,温度不同(T2>T1)、其他条件相同时,下列图象正确的是乙(填代号).

(2)用活性炭还原法也可以处理氮氧化物,某研究小组向某密闭容器加入一定量的活性炭和NO,发生反应C(s)+2NO(g)?N2(g)+CO2(g)△H在T1℃时,反应进行到不同时间测得各物质的量浓度如下:
| 浓度/mol.L-1/时间/min | 0 | 10 | 20 | 30 | 40 | 50 |
| NO | 1.0 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
| N2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
| CO2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
②30min后,只改变某一条件,根据上表的数据判断改变的条件可能是bc(填字母代号).
a.加入一定量的活性炭 b.通入一定量的NO
c.适当缩小容器的体积 d.加入合适的催化剂
③若30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为5:3:3,则达到新平衡时NO的转化率 (填“升高”或“降低”),△H<0(填“>”或“<”).
(3)以CO2与NH3为原料可合成化肥尿素[化学式为CO(NH2)2].已知:
①2NH3(g)+CO2(g)=NH2CO2NH4(s)△H=-l59.5kJ/mol
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g)△H=+116.5kJ/mol
③H2O(l)=H2O(g)△H=+44.0kJ/mol
写出CO2与NH3合成尿素和液态水的热化学反应方程式2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(l)△H=-87.0 kJ•mol-1.
(4)一种氨燃料电池,使用的电解质溶液是2mol/L-1的KOH溶液.
电池反应为:4NH3+3O2=2N2+6H2O;

请写出通入a气体一极的电极反应式为2NH3+6OH--6e-=N2+6H2O;每消耗3.4g NH3转移电子的物质的量为0.6 mol.
18.下列说法正确的是( )
| A. | 实验时皮肤受碱腐蚀,先用大量水冲洗,再用2%醋酸溶液或硼酸溶液洗,最后用水冲洗 | |
| B. | 萃取操作时,要快速振摇分液漏斗,放气时支管口不能对着人,也不能对着火 | |
| C. | 淀粉溶液中加入稀硫酸,加热后再加入适量银氨溶液,水浴加热,可以判断淀粉是否水解 | |
| D. | 液态溴乙烷中加入NaOH溶液共热几分钟,然后滴加AgNO3溶液,可以检验溴乙烷中含溴元素 |
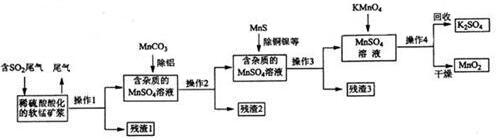
5.碳酸镍可用于电镀、陶瓷器着色等.镍矿渣中镍元素的主要存在形式是Ni(OH)2和NiS(含有Fe、Cu、Ca、Mg、Zn等元素杂质),从镍矿渣出发制备碳酸镍的流程如下:
已知:常温下,部分物质的溶度积常数如表:
(1)浸取过程中欲加快浸取速率,可采用的措施之一是将矿石粉碎(或提高浸取时的温度,或适当增大酸的浓度等合理答案均可);
(2)浸取出Ni2+时反应的离子方程式有①Ni(OH)2+2H+=Ni2++2H2O②NiS+ClO3-+H+→Ni2++S+Cl-+H2O(未配平),此反应中还原产物与氧化产物的物质的量比为1:3.
(3)加入Na2CO3溶液沉铁时生成难溶于水的黄钠铁矾[NaFe3(SO4)2(OH)6]和一种无色气体.写出此反应的离子方程式:3Fe3++3CO32-+Na++2SO42-+3H2O=NaFe3(SO4)2(OH)6+3CO2↑.
(4)加入NiS的作用是除去溶液中的Cu2+,反应的离子方程式为:Cu2++NiS=Ni2++CuS,过滤后,溶液中c(Ni2+)=0.107 mol•L-1时,溶液中残留c(Cu2+)为1.27×10-16mol•L-1.
(5)加入NaF的作用是除去Ca2+,有机萃取剂用于除去Zn2+.

已知:常温下,部分物质的溶度积常数如表:
难溶物 | NiS | ZnS | CuS | CaF2 | MgF2 |
| 溶度积常数 | 1.07×10-21 | 2.93×10-25 | 1.27×10-36 | 1.46×10-10 | 7.42×10-11 |
(2)浸取出Ni2+时反应的离子方程式有①Ni(OH)2+2H+=Ni2++2H2O②NiS+ClO3-+H+→Ni2++S+Cl-+H2O(未配平),此反应中还原产物与氧化产物的物质的量比为1:3.
(3)加入Na2CO3溶液沉铁时生成难溶于水的黄钠铁矾[NaFe3(SO4)2(OH)6]和一种无色气体.写出此反应的离子方程式:3Fe3++3CO32-+Na++2SO42-+3H2O=NaFe3(SO4)2(OH)6+3CO2↑.
(4)加入NiS的作用是除去溶液中的Cu2+,反应的离子方程式为:Cu2++NiS=Ni2++CuS,过滤后,溶液中c(Ni2+)=0.107 mol•L-1时,溶液中残留c(Cu2+)为1.27×10-16mol•L-1.
(5)加入NaF的作用是除去Ca2+,有机萃取剂用于除去Zn2+.
2.短周期主族元素X、Y、Z、W的原子序数依次增大.X、Y、Z、W原子的最外层电子数之和为18,X原子的最外层电子数是其内层电子数的2倍,Y是地壳中含量最高的元素,Z2+与Y2-具有相同的电子层结构.下列说法正确的是( )
| A. | 单质的沸点:Y>Z | |
| B. | X、Y、Z三种元素不可能形成离子化合物 | |
| C. | X的最高价氧化物对应的水化物的酸性比W的强 | |
| D. | Y分别与Z、W形成的化合物中化学键类型不相同 |
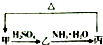 甲、乙、丙三种物质之间有如下转化关系(如图):
甲、乙、丙三种物质之间有如下转化关系(如图):