题目内容
4. 金属镁在目前的汽车、航天、航空、机械制造、军事等产业中得到迅猛发展.
金属镁在目前的汽车、航天、航空、机械制造、军事等产业中得到迅猛发展.(1)目前市场上某些品牌笔记本电脑(如神舟电脑、IBM电脑等)的外壳一改以往的有机合成材料,而使用镁铝合金、钛铝合金等材料.镁铝合金材料在电脑上代替有机合成材料的目的是BC(多选).
A.降低成本 B.增强美观 C.利于散热
D.增加强度E.增加运算速度
(2)某学校研究性学习小组欲以镁条、铝片为电极,以稀NaOH溶液为电解质溶液设计原电池.
①给你一只安培表,请你画出该原电池的示意图,并标出正负极.
②一段时间后,铝片发生的电极反应式是Al+4OH--3e-=AlO2-+2H2O;镁条表面有气泡产生,则镁条的电极反应式为2H++2e-═H2↑;总的离子方程式是2Al+2OH-+2H2O=2AlO2-+3H2↑.
分析 (1)根据铝合金材料(有钛铝合金、镁铝合金等)硬度大,而且美观分析;
(2)①Mg虽比Al活泼,但Mg不能与NaOH溶液反应,而Al可与NaOH溶液反应,故Al作负极,Mg做正极;
②Al作负极,失电子生成Al3+,Al3+结合OH-生成AlO2-,镁做正极,氢离子在正极得到电子被还原.
解答 解:(1)因为铝合金材料(有钛铝合金、镁铝合金等)硬度大,而且美观,所以铝合金材料在电脑上代替有机合成材料,
故选:BC;
(2)①Mg虽比Al活泼,但Mg不能与NaOH溶液反应,而Al可与NaOH溶液反应,故Al作负极,Mg做正极;原电池装置图: ;
;
故答案为: ;
;
②随后阶段,负极是铝,电极反应式:Al+4OH--3e-=AlO2-+2H2O,正极是镁,镁条表面有气泡产生,电极反应式:2H++2e-═H2↑,总的离子方程式是故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑;
故答案为:Al+4OH--3e-=AlO2-+2H2O;2H++2e-═H2↑;2Al+2OH-+2H2O=2AlO2-+3H2↑.
点评 本题考查了元素化合物的性质,侧重考查镁铝的性质,熟悉合金的概念及性质,明确原电池构成条件是解题关键,题目难度中等.

练习册系列答案
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案
相关题目
14.下列表示物质结构的化学用语正确的是( )
| A. | 甲烷分子的比例模型: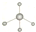 | B. | 苯的最简式:CH | ||
| C. | 乙烯的分子式:CH2=CH2 | D. | 乙醇的结构简式:C2H6O |
15.能正确表示下列反应的离子方程式是( )
| A. | 向氨水中通入足量二氧化碳:NH3•H2O+CO2═NH4++HCO3- | |
| B. | 铜片与浓硝酸反应:Cu+NO3-+4H+═Cu2++NO2↑+2H2O | |
| C. | 氯化铵浓溶液跟NaOH浓溶液混合后加热:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3•H2O | |
| D. | 84消毒液具有消毒性的原理为:2ClO-+CO2+H2O=2HClO+CO32- |
19.如图实验装置或操作不符合实验要求的是( )
| A. |  石油分馏 | B. |  灼烧干海带 | ||
| C. |  用CCl4萃取碘水中的碘 | D. |  治炼金属铁 |
13.下列各组物质的无色溶液,不用其它试剂即可鉴别的是( )
①KCl Na2CO3 HCl ②NaHCO3 Ba(OH)2 H2SO4
③HCl NaAlO2 NaHSO4 ④Ca(OH)2 Na2CO3 BaCl2.
①KCl Na2CO3 HCl ②NaHCO3 Ba(OH)2 H2SO4
③HCl NaAlO2 NaHSO4 ④Ca(OH)2 Na2CO3 BaCl2.
| A. | ①② | B. | ②③ | C. | ①③④ | D. | ①②④ |
14.在化学实验室进行下列实验操作时,其操作或记录的数据正确的是( )
| A. | 用托盘天平称取8.84 g食盐 | |
| B. | 用220 mL容量瓶配制所需的220 mL 0.1 mol/L NaOH溶液 | |
| C. | 用量筒量取12.12 mL盐酸 | |
| D. | 用0.1200 mol/L盐酸滴定未知浓度的NaOH溶液,消耗盐酸21.40 mL |
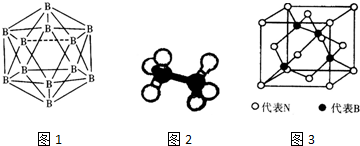
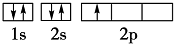 ,核外有5种运动状态不同的电子.
,核外有5种运动状态不同的电子.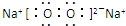 .
.