题目内容
20.下列反应中,属于氧化还原反应的是( )| A. | 2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$ Na2CO3+CO2↑+H2O | B. | H2SO4+CuO═CuSO4+H2O | ||
| C. | 2 H2S+SO2═3S↓+2H2O | D. | CO2+Ca(OH)2═CaCO3↓+H2O |
分析 氧化还原反应的实质为电子转移、特征为化合价升降,所以氧化还原反应中一定存在元素化合价变化,据此对各选项进行判断.
解答 解:A.2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$ Na2CO3+CO2↑+H2O为分解反应,反应中不存在化合价变化,不属于氧化还原反应,故A错误;
B.H2SO4+CuO═CuSO4+H2O为复分解反应,不存在化合价变化,不属于氧化还原反应,故B错误;
C.2 H2S+SO2═3S↓+2H2O,存在S元素化合价变化,属于氧化还原反应,故C正确;
D.CO2+Ca(OH)2═CaCO3↓+H2O为复分解反应,不存在化合价变化,不属于氧化还原反应,故D错误;
故选C.
点评 本题考查了氧化还原反应的判断,题目难度不大,明确氧化还原反应的实质、特征为解答关键,注意掌握四种基本反应类型与氧化还原反应之间的关系,试题有利于提高学生的灵活应用能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
10.甲醇是一种重要的化工原料,又是一种可再生能源,具有开发和应用的广阔前景.
(1)已知:
CH3OH(g)=HCHO(g)+H2(g)△H=+84kJ•mol-1
2H2(g)+O2(g)═2H2O(g)△H=-484kJ•mol-1
工业上常以甲醇为原料制取甲醛,请写出CH3OH(g)与O2(g)反应生成HCHO(g)和H2O(g)的热化学方程式:2CH3OH(g)+O2(g)=2HCHO(g)+2H2O(g)△H=-316 kJ•mol-1.
(2)工业上可用如下方法合成甲醇,化学方程式为CO(g)+2H2(g)?CH3OH(g),已知某些化学键的键能数据如表:
请回答下列问题
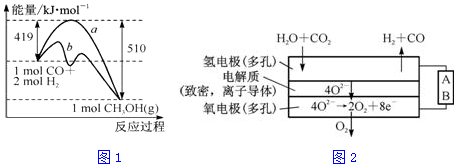
①该反应的△S<(填“>”或“<”)0.图1中曲线a到曲线b的措施是加入催化剂.
②已知CO中的C与O之间为三键,其键能为x kJ•mol-1,则x=1097.
(3)由甲醇、氧气和NaOH溶液构成的新型手机电池,可使手机连续使用一个月才充一次电.①该电池负极的电极反应式为CH3OH-6e-+8OH-=CO32-+6H2O.
②若以该电池为电源,用石墨作电极电解200mL含有如表离子的溶液.
电解一段时间后,当两极收集到相同体积(相同条件下)的气体时(忽略溶液体积的变化及电极产物可能存在的溶解现象)阳极上收集到氧气的质量为3.2g.
(4)电解水蒸气和CO2产生合成气(H2+CO).较高温度下(700~1 000℃),在SOEC两侧电极上施加一定的直流电压,H2O和CO2在氢电极发生还原反应产生O2-,O2-穿过致密的固体氧化物电解质层到达氧电极,在氧电极发生氧化反应得到纯O2.由图2可知A为直流电源的负极(填“正极”或“负极”),请写出以H2O为原料生成H2的电极反应式:H2O+2e-=H2↑+O2-.
(1)已知:
CH3OH(g)=HCHO(g)+H2(g)△H=+84kJ•mol-1
2H2(g)+O2(g)═2H2O(g)△H=-484kJ•mol-1
工业上常以甲醇为原料制取甲醛,请写出CH3OH(g)与O2(g)反应生成HCHO(g)和H2O(g)的热化学方程式:2CH3OH(g)+O2(g)=2HCHO(g)+2H2O(g)△H=-316 kJ•mol-1.
(2)工业上可用如下方法合成甲醇,化学方程式为CO(g)+2H2(g)?CH3OH(g),已知某些化学键的键能数据如表:
| 化学键 | C-C | C-H | H-H | C-O | C≡O | O-H |
| 键能/kJ•mol-1 | 348 | 413 | 436 | 358 | x | 463 |

①该反应的△S<(填“>”或“<”)0.图1中曲线a到曲线b的措施是加入催化剂.
②已知CO中的C与O之间为三键,其键能为x kJ•mol-1,则x=1097.
(3)由甲醇、氧气和NaOH溶液构成的新型手机电池,可使手机连续使用一个月才充一次电.①该电池负极的电极反应式为CH3OH-6e-+8OH-=CO32-+6H2O.
②若以该电池为电源,用石墨作电极电解200mL含有如表离子的溶液.
| 离子 | Cu2+ | H+ | Cl- | SO42 - |
| c/mol•L-1 | 0.5 | 2 | 2 | 0.5 |
(4)电解水蒸气和CO2产生合成气(H2+CO).较高温度下(700~1 000℃),在SOEC两侧电极上施加一定的直流电压,H2O和CO2在氢电极发生还原反应产生O2-,O2-穿过致密的固体氧化物电解质层到达氧电极,在氧电极发生氧化反应得到纯O2.由图2可知A为直流电源的负极(填“正极”或“负极”),请写出以H2O为原料生成H2的电极反应式:H2O+2e-=H2↑+O2-.
11.可用来鉴别乙醇、乙醛的试剂是( )
| A. | 银氨溶液 | B. | 乙酸溶液 | C. | 氯化铁溶液 | D. | 氢氧化钠溶液 |
8.生活中下列物质起还原作用的是( )
| A. | 明矾作净水剂 | B. | 硅胶作干燥剂 | C. | 铁粉作脱氧剂 | D. | 活性炭作吸附剂 |
15.下列粒子的结构示意图中,表示钠原子的是( )
| A. | 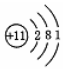 | B. | 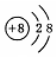 | C. | 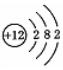 | D. | 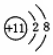 |
5.同主族元素形成的同一类型化合物,往往其结构和性质相似.PH4I是一种白色晶体,下列对PH4I的叙述中,正确的是( )
| A. | 它是一种共价化合物 | |
| B. | 它只含共价键 | |
| C. | 它不可能与NaOH溶液反应 | |
| D. | 它受热时,可能会分解产生有色气体 |
12.NA代表阿伏加德罗常数,下列说法正确的是( )
| A. | 通入了1 molCl2的新制氯水中,HClO、Cl-、C1O-粒子数之和为2NA | |
| B. | 标准状况下,22.4L NH3和HCl的混合气体中含有的分子总数为NA | |
| C. | 常温下,pH=2的H2SO4溶液中含有的H+数目为0.02NA | |
| D. | 高温下,0.3mol Fe与足量的水蒸气完全反应失去的电子数为0.8NA |
9. 磷酸铁锂(LiFePO4)电池是一种高效、环保的新型电池,装置如图所示,其中正极材料橄榄石型LiFePO4通过粘合剂附着在铝箔表面,负极石墨材料附着在铜箔表面,电解质为溶解在有机溶剂中的锂盐,电池工作时的总反应为:LiFePO4+6C $?_{放电}^{充电}$Li1-xFePO4+LixC6,则下列说法错误的是( )
磷酸铁锂(LiFePO4)电池是一种高效、环保的新型电池,装置如图所示,其中正极材料橄榄石型LiFePO4通过粘合剂附着在铝箔表面,负极石墨材料附着在铜箔表面,电解质为溶解在有机溶剂中的锂盐,电池工作时的总反应为:LiFePO4+6C $?_{放电}^{充电}$Li1-xFePO4+LixC6,则下列说法错误的是( )
 磷酸铁锂(LiFePO4)电池是一种高效、环保的新型电池,装置如图所示,其中正极材料橄榄石型LiFePO4通过粘合剂附着在铝箔表面,负极石墨材料附着在铜箔表面,电解质为溶解在有机溶剂中的锂盐,电池工作时的总反应为:LiFePO4+6C $?_{放电}^{充电}$Li1-xFePO4+LixC6,则下列说法错误的是( )
磷酸铁锂(LiFePO4)电池是一种高效、环保的新型电池,装置如图所示,其中正极材料橄榄石型LiFePO4通过粘合剂附着在铝箔表面,负极石墨材料附着在铜箔表面,电解质为溶解在有机溶剂中的锂盐,电池工作时的总反应为:LiFePO4+6C $?_{放电}^{充电}$Li1-xFePO4+LixC6,则下列说法错误的是( )| A. | 装置中的聚合物隔膜应为阳离子交换膜 | |
| B. | 充电时,Li+迁移方向为由右向左 | |
| C. | 充电时,LiFePO4中的铁元素被氧化 | |
| D. | 放电时,正极的电极反应式为:Li1-xFePO4+xLi++xe-═LiFePO4 |
10.以炼锌烟尘(主要成份为ZnO,含少量CuO和FeO)为原料,可以制取氧化锌和金属锌.
Ⅰ.制取氧化锌主要工艺如图1:
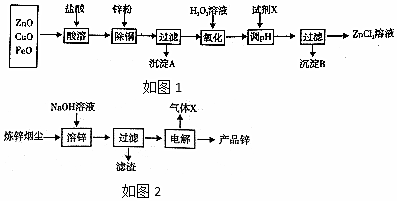
表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为l.0mol/L计算).
(1)为了加快反应,“酸溶”需要适当加热,但温度不宜太高,原因是减少盐酸挥发.
(2)加入H2O2溶液发生反应的离子方程式2Fe2++H2O2+2H+=2Fe3++2H2O.
(3)流程图中,为了降低溶液的酸度,调节pH范围为3.2≤PH<5.2;若试剂X为Zn2(OH)2CO3,加入X除杂质的离子方程式为3Zn2(OH)2CO3+4Fe3++3H2O=4Fe(OH)3↓+6Zn2++3CO2↑.
(4)已知,室温下,Ksp[Fe(OH)3]=4.0×10-38,当pH=3时,溶液中c(Fe3+)为4.0×10-5.从ZnCl2溶液中提取无水ZnCl2的方法是在氯化氢气体,蒸干氯化锌溶液并加热至失去结晶水.
Ⅱ.制取金属锌采用碱溶解ZnO(s)+2NaOH (aq)+H2O═Na2[Zn(OH)4](aq),然后电解浸取液.
(5)如图2,炼锌烟尘采用碱溶,而不采用酸溶后电解,主要原因是氧化铜、氧化亚铁不溶于碱溶液中.
(6)以石墨作电极电解时,阳极产生的气体为O2;阴极的电极反应为[Zn(OH)4]2-+2e-=Zn+4OH-.
Ⅰ.制取氧化锌主要工艺如图1:

表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为l.0mol/L计算).
| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 1.1 | 3.2 |
| Zn2+ | 5.2 | 6.4 |
| Fe2+ | 5.8 | 8.8 |
(2)加入H2O2溶液发生反应的离子方程式2Fe2++H2O2+2H+=2Fe3++2H2O.
(3)流程图中,为了降低溶液的酸度,调节pH范围为3.2≤PH<5.2;若试剂X为Zn2(OH)2CO3,加入X除杂质的离子方程式为3Zn2(OH)2CO3+4Fe3++3H2O=4Fe(OH)3↓+6Zn2++3CO2↑.
(4)已知,室温下,Ksp[Fe(OH)3]=4.0×10-38,当pH=3时,溶液中c(Fe3+)为4.0×10-5.从ZnCl2溶液中提取无水ZnCl2的方法是在氯化氢气体,蒸干氯化锌溶液并加热至失去结晶水.
Ⅱ.制取金属锌采用碱溶解ZnO(s)+2NaOH (aq)+H2O═Na2[Zn(OH)4](aq),然后电解浸取液.
(5)如图2,炼锌烟尘采用碱溶,而不采用酸溶后电解,主要原因是氧化铜、氧化亚铁不溶于碱溶液中.
(6)以石墨作电极电解时,阳极产生的气体为O2;阴极的电极反应为[Zn(OH)4]2-+2e-=Zn+4OH-.