题目内容
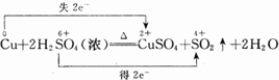
在Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O 反应中,
CuSO4+SO2↑+2H2O
 .
.
| ||
Cu
Cu
元素被氧化,电子转移的总数为2e-
2e-
.请用双线桥表示该反应的电子转移方向和数目.Cu+2H2SO4(浓)
| ||


分析:Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O中,Cu元素的化合价升高,S元素的化合价降低,以此来解答.
| ||
解答:解:Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O中,Cu元素的化合价升高,S元素的化合价降低,
则Cu失去电子,被氧化,该反应中转移2e-,
铜失去两个电子,硫酸中硫得到两个电子,则双线桥表示该反应的电子转移方向和数目为 ,
,
故答案为:Cu;2e-; .
.
| ||
则Cu失去电子,被氧化,该反应中转移2e-,
铜失去两个电子,硫酸中硫得到两个电子,则双线桥表示该反应的电子转移方向和数目为
 ,
,故答案为:Cu;2e-;
 .
.点评:本题考查氧化还原反应,为高考常见题型,侧重基本概念的考查,注意把握反应中元素的化合价变化为解答的关键,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目