题目内容
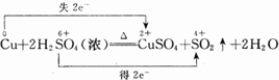
在Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O反应中
(1)
(2)用双线桥标出该反应电子转移的方向和数目.Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O
(3)若有2.4mol的H2SO4参与反应,则被还原的H2SO4为
| ||
(1)
铜
铜
元素被氧化,硫酸
硫酸
是氧化剂.(2)用双线桥标出该反应电子转移的方向和数目.Cu+2H2SO4(浓)
| ||
(3)若有2.4mol的H2SO4参与反应,则被还原的H2SO4为
117.6
117.6
g.分析:(1)失电子化合价升高的元素被氧化,得电子化合价降低的反应物是氧化剂;
(2)铜失电子数=1(2-0)=2,硫酸得电子数=1(6-4)=2,该反应中转移电子数是2,用用双线桥标出该反应电子转移的方向和数目;
(3)根据参加反应的和参加氧化还原反应的硫酸之间的关系式计算.
(2)铜失电子数=1(2-0)=2,硫酸得电子数=1(6-4)=2,该反应中转移电子数是2,用用双线桥标出该反应电子转移的方向和数目;
(3)根据参加反应的和参加氧化还原反应的硫酸之间的关系式计算.
解答:解:(1)Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O中,铜元素的化合价由0价→+2价,失电子被氧化,硫元素的化合价由+6价→+4价,所以硫酸得电子作氧化剂,故答案为:铜;硫酸;
(2)铜失电子数=1(2-0)=2,硫酸得电子数=1(6-4)=2,该反应中转移电子数是2,用用双线桥标出该反应电子转移的方向和数目为: ,故答案为:
,故答案为: ;
;
(3)该反应中有一半的硫酸是氧化剂,一半的硫酸起酸的作用,所以若有2.4mol的H2SO4参与反应,则被还原的H2SO4的物质的量是1.2mol,其质量=1.2mol×98g/mol=117.6g,
故答案为:117.6.
| ||
(2)铜失电子数=1(2-0)=2,硫酸得电子数=1(6-4)=2,该反应中转移电子数是2,用用双线桥标出该反应电子转移的方向和数目为:
 ,故答案为:
,故答案为: ;
;(3)该反应中有一半的硫酸是氧化剂,一半的硫酸起酸的作用,所以若有2.4mol的H2SO4参与反应,则被还原的H2SO4的物质的量是1.2mol,其质量=1.2mol×98g/mol=117.6g,
故答案为:117.6.
点评:本题考查氧化还原反应,明确元素化合价变化是解本题关键,难点是标电子转移的方向和数目,注意箭头的指向.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目