题目内容
在一个固定容积的密闭容器中,保持一定的温度,在一定条件下进行以下反应:?A(g)+3B(g)(1)达到平衡时C在反应混合气体中的百分含量是______________(用含有a的关系式表示)。
(2)在相同的实验条件下,若在同一个容器中改为加入2 mol A和6 mol B,达到平衡后,?C的物质的量为______________mol,此时C在混合气体中的百分含量______________(填“增大”“减小”或“不变”)。
(3)若在同一个容器中改为加入2 mol A和3 mol B,能否通过调节C的物质的量,使平衡时C在混合气体中的百分含量与原平衡相同?(如果能,请写出C的物质的量,如不能,请说明通过什么方法可以实现)。
(4)在相同实验条件下,如果加入n mol A、m mol B和p mol C,若要求平衡后C在混合气体中的百分含量保持不变,则n、m与p的关系是_________________________________。
(1)[3(1—a)/(3+a)]×100%
(2)大于6(1-a) 增大
(3)不能,可通过调节温度来实现。
(4)n+![]() =1,m+p=3
=1,m+p=3
解析:(1)平衡时A的物质的量为a mol,说明参加反应的A为(1-a) mol,利用化学方程式可计算出平衡时C的物质的量为3(1-a) mol,C在反应混合气体中的百分含量是[3(1-a)/(3+a)]×100%
(2)在同一个容器中改为加入2 mol A和6 mol B,相当于原混合体系加压使压强增至原来的2倍,平衡右移,所以C的浓度比原来的2倍还要大,即大于6(1-a),C在混合气体中的百分含量增大。
(3)若在同一个容器中改为加入2 mol A和3 mol B,不管C的物质的量为多少,平衡时C在混合气体中的百分含量与原平衡时都不可能相同。因为我们可以先将C转化为A,这样便可看出A与B的物质的量都不可能为1 mol A和3 mol B,也就是C的百分含量要发生改变。可通过调节温度来实现。
(4)可将C转化为反应物A和B,由于容器的体积不变,要使C的百分含量不变,必须保证A、B的起始量与原起始量相同。所以n+![]() =1,m+p=3。
=1,m+p=3。

 应用题作业本系列答案
应用题作业本系列答案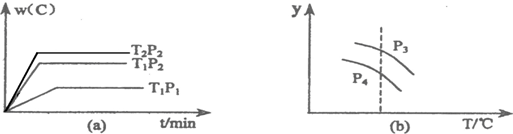
| A、P3>P4,y轴表示A的转化率 | B、P3<P4,y轴表示B的体积分数 | C、P3>P4,y轴表示混合气体的平均相对分子质量 | D、P3>P4,y轴表示混合气体的密度 |
| A、a:b:c=m:n:p | ||||||
B、a:b=m:n,
| ||||||
C、
| ||||||
D、a=
|
 2C(g),起始加入1molA和2molB,反应达到平衡后测得C的浓度为p mol/L,且C的体积分数为ω.在相同条件下:
2C(g),起始加入1molA和2molB,反应达到平衡后测得C的浓度为p mol/L,且C的体积分数为ω.在相同条件下: 2SO3(g),(正反应是放热反应),达到平衡后,其它条件不变时,只改变下列的某一个条件,将变化的情况(增大、减小、不变)填入空格中.
2SO3(g),(正反应是放热反应),达到平衡后,其它条件不变时,只改变下列的某一个条件,将变化的情况(增大、减小、不变)填入空格中. 化学学科中的平衡理论主要内容包括:化学平衡、电离平衡、水解平衡和溶解平衡等四种.且均符合勒夏特列原理.请回答下列问题.
化学学科中的平衡理论主要内容包括:化学平衡、电离平衡、水解平衡和溶解平衡等四种.且均符合勒夏特列原理.请回答下列问题.