题目内容
4.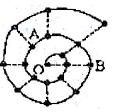 某同学在研究前18号元素时发现,可以将它们排成如图所示的“蜗牛”形状,图中每个“•”代表一种元素,其中O点代表氢元素.下列说法中错误的是( )
某同学在研究前18号元素时发现,可以将它们排成如图所示的“蜗牛”形状,图中每个“•”代表一种元素,其中O点代表氢元素.下列说法中错误的是( )| A. | A、B组成的化合物中不可能含有共价键 | |
| B. | 虚线相连的元素处于同一族 | |
| C. | B元素是图中金属性最强的元素 | |
| D. | 离O点越远的元素原子半径越大 |
分析 O点代表氢元素,按照原子序数由小到大由里往外延伸,由图可知,O、B连线的三元素为第ⅠA族,A为O元素,B为Na元素,C为Al元素,根据元素的种类可知虚线相连的元素处于同一族,结合对应元素的性质解答该题.
解答 解:A.钠与氧元素可以形成过氧化钠,过氧根离子中氧原子之间为共价键,故A错误;
B.由原子序数可知,虚线相连的元素处于同一族,故B正确;
C.B为Na元素,是图中金属性最强的元素,故C正确;
D.离O点越远的元素原子的核电荷数增大,若电子层相同,半径越小,故D错误;
故选AD.
点评 本题考查位置、结构与性质关系的应用,题目难度不大,看懂图象推断元素是解题的关键,注意对元素周期表的整体把握.

练习册系列答案
相关题目
14.只含有极性共价键的物质是( )
| A. | NH3 | B. | CaCl2 | C. | Cl2 | D. | K2S |
15.表是元素周期表的一部分,已知⑤为短周期元素,其单质为淡黄色固体,据表回答有关问题:
(1)画出元素⑧的原子结构示意图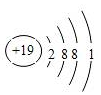
(2)在这些元素中,最活泼的非金属元素是F,最不活泼的元素是Ar(写元素符号 ).
(3)在这些元素的最高价氧化物对应水化物中,碱性最强的是KOH(写化学式),呈两性的氢氧化物是Al(OH)3(写化学式),写出两者之间反应的离子方程式:Al(OH)3+OH-=AlO2-+2H2O
(4)在⑥与⑨中,化学性质较活泼的是Cl(写元素符号 ),写出可以验证该结论的一个化学反应方式Cl2+2NaBr=Br2+2NaCl.
| ① | ② | ||||||
| ③ | ④ | ⑤ | ⑥ | ⑦ | |||
| ⑧ | ⑨ |

(2)在这些元素中,最活泼的非金属元素是F,最不活泼的元素是Ar(写元素符号 ).
(3)在这些元素的最高价氧化物对应水化物中,碱性最强的是KOH(写化学式),呈两性的氢氧化物是Al(OH)3(写化学式),写出两者之间反应的离子方程式:Al(OH)3+OH-=AlO2-+2H2O
(4)在⑥与⑨中,化学性质较活泼的是Cl(写元素符号 ),写出可以验证该结论的一个化学反应方式Cl2+2NaBr=Br2+2NaCl.
12.为实现实验目的,选用的装置、实验操作均正确的是( )
| 实验目的 | 实验步骤和装置 | |
| A | 验证SO2具有漂白性 | 将SO2通入氢氧化钠的酚酞试液中 |
| B | 探究温度对反应速率的影响 | 不同温度下,取0.1 mol/LKI 溶液,向其中先加入淀粉溶液,再加入0.1 mol/L 硫酸,记录溶液出现蓝色的时间 |
| C | 验证牺牲阳极的阴极保护法 | 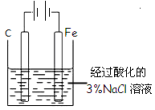 往铁电极附近滴加铁氰化钾溶液 |
| D | 检验蔗糖水解产物具有还原性 | 向蔗糖溶液中加入几滴稀硫酸,水浴加热几分钟,再向其中加入新制的Cu(OH)2,加热3-5min. |
| A. | A | B. | B | C. | C | D. | D |
2.Cu粉放入稀H2SO4中,加热后无现象,当加入一种盐后,Cu粉质量减少,而溶液变蓝,同时有气体生成,此盐是( )
| A. | 氯化物 | B. | 硫酸盐 | C. | 硝酸盐 | D. | 碳酸盐 |
9.一定量的稀硫酸和过量铁块反应时,为了加快反应速率,且不影响生成氢气的总量,下列措施不正确的是( )
| A. | 改用浓硫酸 | B. | 加热 | ||
| C. | 加入少量CuSO4固体 | D. | 将铁块改成铁粉 |