题目内容
19.下列各组物质分类正确的是( )| 电解质 | 非电解质 | 化合物 | |
| A | H2SO4 | Cl2 | NaCl |
| B | NaOH | 酒精 | N2 |
| C | CuSO4 | 水银 | CO2 |
| D | BaSO4 | 蔗糖 | KClO3 |
| A. | A | B. | B | C. | C | D. | D |
分析 在水溶液里或熔融状态下能导电的化合物是电解质,包括酸、碱、盐、活泼金属氧化物和水;
在水溶液里和熔融状态下都不能导电的化合物是非电解质,包括一些非金属氧化物、氨气、大多数有机物(如蔗糖、酒精等);
由不同元素组成的纯净物属于化合物,由同种元素组成的纯净物是单质;
解答 解:A.氯气为单质,既不是电解质,也不是非电解质,故A错误;
B.NaOH是电解质,酒精是非电解质,N2是单质,故B错误;
C.CuSO4是电解质;水银是单质,不是非电解质,二氧化碳是化合物,故B错误;
D.BaSO4是电解质;蔗糖是非电解质,KClO3是化合物,故D正确;
故选:D.
点评 本题考查了化学的基本概念,书写电解质、非电解质、化合物的概念是解题关键,注意单质、混合物既不是电解质也不是非电解质,题目难度不大.

练习册系列答案
 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案
相关题目
9.下列有关氧化还原反应的叙述正确的是( )
| A. | 化合反应和复分解反应不可能是氧化还原反应 | |
| B. | 阳离子只能得到电子被还原,阴离子只能失去电子被氧化 | |
| C. | 含有最高价元素的化合物不一定具有很强的氧化性 | |
| D. | 在氧化还原反应中肯定有一种元素被氧化,另一种元素被还原 |
10.在温度相同、体积均为1L的三个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下.已知:2SO2(g)+O2(g)?2SO3(g)△H=-98.3kJ•mol-1.
则:α1+α2=1,p=1.6mol,b+c=39.32kJ.
| 容 器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 2mol SO2、1mol O2 | 2mol SO3 | m mol SO2、n mol O2、p mol SO3 |
| c(SO3)/mol•L-1 | 1.4 | 1.4 | 1.4 |
| 能量变化 | 放出a kJ | 吸收b kJ | 吸收c kJ |
| SO2或SO3的转化率 | α1 | α2 | 12.5% |
7.下列说法正确的是( )
| A. | 在标准状况下,1mol水和1molH2的体积都约是22.4L | |
| B. | 2gH2和44gCO2的体积相等 | |
| C. | 1mol某气体的体积为22.4L,则该气体一定处于标准状况 | |
| D. | 在标准状况下,1gH2和11.2LO2的物质的量相等 |
14.食盐、纯碱(Na2CO3)、食醋均为厨房中常用的物质,利用这些物质不能实现的实验是( )
①除去热水瓶内壁的水垢(CaCO3) ②检验自来水中是否含有氯离子
③检验镁粉中是否含有锌粉 ④鉴别食盐和纯碱(Na2CO3)
①除去热水瓶内壁的水垢(CaCO3) ②检验自来水中是否含有氯离子
③检验镁粉中是否含有锌粉 ④鉴别食盐和纯碱(Na2CO3)
| A. | ①④ | B. | ②③ | C. | ②④ | D. | ①② |
4.氯化铵是一种重要化工原料,也是一种常用的氨肥.
(1)氯化铵作为化肥时不宜与草木灰(主要成分K2CO3)混用.其原因是氯化铵与碳酸钾发生相互促进的水解反应生成氨气,会降低肥效.
(2)热的浓氯化铵溶液可以清洗铁器表面锈迹,写出相关反应的离子方程式:6NH4++Fe2O3$\frac{\underline{\;加热\;}}{\;}$2Fe3++6NH3↑+3H2O.
(3)常温下,在20mLamol.L-1氨水中滴加加20mLbmol.L-1HCl溶液恰好至溶液呈中性.计算常温下,NH3.H2O的电离常数Kb=$\frac{a}{a-b}$×10-7mol/L(用含a,b的精确代数式表示)
(4)为了探究外界条件对氯化铵水解平衡的影响,设计如下实验方案:
限选药品和仪器:恒温水浴、pH计、烧杯、0.1mol.L-1硝酸银溶液、蒸馏水和各种浓度的NH4Cl溶液.
①实验中,“待测物理量”是溶液的pH.
②i=30;ii:探究温度对氯化铵水解平衡的影响.
③上述表格中,y>(填“>”“<”或“=”)m.
(1)氯化铵作为化肥时不宜与草木灰(主要成分K2CO3)混用.其原因是氯化铵与碳酸钾发生相互促进的水解反应生成氨气,会降低肥效.
(2)热的浓氯化铵溶液可以清洗铁器表面锈迹,写出相关反应的离子方程式:6NH4++Fe2O3$\frac{\underline{\;加热\;}}{\;}$2Fe3++6NH3↑+3H2O.
(3)常温下,在20mLamol.L-1氨水中滴加加20mLbmol.L-1HCl溶液恰好至溶液呈中性.计算常温下,NH3.H2O的电离常数Kb=$\frac{a}{a-b}$×10-7mol/L(用含a,b的精确代数式表示)
(4)为了探究外界条件对氯化铵水解平衡的影响,设计如下实验方案:
| 实验序号 | c(NH4Cl)/mol.L-1 | 温度/℃ | 待测物理量 | 实验目的 |
| Ⅰ | 0.5 | 30 | x | - |
| Ⅱ | 1.5 | i | y | 探究浓度对氯化铵水解平衡的影响 |
| Ⅲ | 0.5 | 35 | z | ii |
| Ⅳ | 2.0 | 40 | m | 探究温度、浓度同时对氯化铵水解平衡的影响 |
①实验中,“待测物理量”是溶液的pH.
②i=30;ii:探究温度对氯化铵水解平衡的影响.
③上述表格中,y>(填“>”“<”或“=”)m.
2.下列疾病与人体缺乏矿物质元素有关的是( )
| A. | 坏血病 | B. | 夜盲症 | C. | 骨质疏松 | D. | 糖尿病 |
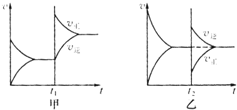 在一定条件下,有反应xA+yB?zC.
在一定条件下,有反应xA+yB?zC.