题目内容
10.在温度相同、体积均为1L的三个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下.已知:2SO2(g)+O2(g)?2SO3(g)△H=-98.3kJ•mol-1.| 容 器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 2mol SO2、1mol O2 | 2mol SO3 | m mol SO2、n mol O2、p mol SO3 |
| c(SO3)/mol•L-1 | 1.4 | 1.4 | 1.4 |
| 能量变化 | 放出a kJ | 吸收b kJ | 吸收c kJ |
| SO2或SO3的转化率 | α1 | α2 | 12.5% |
分析 恒温恒容下,甲、乙、丙中起始投料量不同,平衡时三氧化硫浓度均为1.4mol/L,为完等效平衡,按化学计量数转化到左边满足n(SO2)-2mol、n(O2)=1mol,平衡时同种组分的物质的量相等,体积均为1L,最终n(SO3)=1.4 mol,丙中吸收热量,反应逆向进行建立平衡,再结合SO3的转化率为12.5%计算p的值,进而计算丙中转化的三氧化硫物质的量,再结合热化学方程式计算c;
根据甲容器计算各组分物质的量变化量、平衡时各组分物质的量,可以计算甲、乙中转化率,结合热化学方程式计算b,进而得到甲、乙中转化率之和及热量b、c之和.
解答 解:恒温恒容下,甲、乙、丙中起始投料量不同,平衡时三氧化硫浓度均为1.4mol/L,为完等效平衡,按化学计量数转化到左边满足n(SO2)-2mol、n(O2)=1mol,平衡时同种组分的物质的量相等,体积均为1L,最终n(SO3)=1.4 mol,丙中吸收热量,反应逆向进行建立平衡,
甲容器:2SO2(g)+O2(g)?2SO3(g)
起始量(mol):2 1 0
变化量(mol):1.4 0.7 1.4
变化量(mol):0.6 0.3 1.4
则α1=$\frac{1.4mol}{2mol}$=0.7,
乙容器:α2=$\frac{2mol-1.4mol}{2mol}$=0.3,b=98.3kJ×=$\frac{2mol-1.4mol}{2mol}$=29.49kJ,
丙容器:p=1.4÷(1-12.5%)=1.6,则转化的三氧化硫为1.6mol-1.4mol=0.2mol,故c=98.3kJ×$\frac{0.2mol}{2mol}$=9.83kJ,
故α1+α2=0.7+0.3=1,b+c=29.49+9.83=39.32,
故答案为:1;1.6;39.32.
点评 本题考查化学平衡计算,关键是理解等效平衡规律:1、恒温恒容,反应前后气体体积不等,按化学计量数转化到一边,对应物质满足等量;反应前后气体体积相等,按化学计量数转化到一边,对应物质满足等比,2:恒温恒压,按化学计量数转化到一边,对应物质满足等比.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | FeCl2 | B. | KNO3 | C. | FeSO4 | D. | HCl |
| A. | 对症下药是合理用药的首要原则 | |
| B. | 能被充分、快速吸收而无刺激性的药物,可在饭前口服 | |
| C. | 服药一般用温开水,止咳糖浆也可用水冲服 | |
| D. | 一种药物的用量,是经过严格的科学实验和大量的临床研究确定的 |
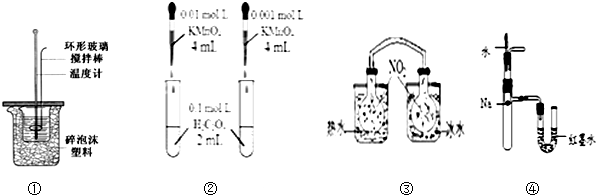
| A. | 装置①用于测定中和热装置 | |
| B. | 装置②依据褪色快慢比较浓度对反应速率的影响 | |
| C. | ③依据两容器内气体颜色变化,判断反应2NO2(g)?N2O4(g)平衡移动的方向 | |
| D. | 装置④依据U管两边液面的高低判断Na和水反应的热效应 |
 氢气是一种新型的绿色能源,又是一种重要的化工原料.
氢气是一种新型的绿色能源,又是一种重要的化工原料.(1)氢气的燃烧热值高,H2(g)+1/2O2 (g)=H2O (g)△H=-241.8kJ•mol-1
| 化学键 | H-H | O=O | O-H |
| 键能(kJ•mol-1) | X | 496.4 | 463 |
(2)根据现代工业技术可以用H2和CO反应来生产燃料甲醇,其反应方程式如下:
CO2 (g)+3H2(g)?H2O(l)+CH3OH(g)△H=-49.00kJ•mol-1
一定温度下,在体积为1L的密闭容器中充入1.00mol CO2和3.00mol H2,测得CO2和CH3OH的浓度随时间变化如图所示.
①能说明该反应已达平衡状态的是A(填代号).
A.CO2在混合气体中的体积分数保持不变
B.单位时间内每消耗1.2mol H2,同时生成0.4mol H2O
C.反应中H2O与CH3OH的物质的量浓度比为1:1,且保持不变
②从反应开始到平衡时的平均反应速率v(H2)=0.225mol/(L.min),达到平衡时氢气的转化率为75%.
③该温度下的平衡常数表达式为$\frac{c(C{H}_{3}OH)}{c(C{O}_{2})×{c}^{3}({H}_{2})}$.
④下列的条件一定能加快反应速率并且提高H2转化率的是D(填代号).
A.降低反应温度
B.分离出水
C.保持容器体积不变,充入稀有气体
D.保持容器体积不变,充入CO2气体.
| A. | BaCl2 Na2CO3 盐酸 AgNO3 | |
| B. | BaCl2 Na2CO3 AgNO3 盐酸 | |
| C. | Na2CO3盐酸 AgNO3 BaCl2 | |
| D. | AgNO3盐酸 BaCl2 Na2CO3 |