题目内容
7.用FeCl3溶液无法区别的一组试剂是( )| A. | KSCN溶液、KCl溶液 | B. | NaOH溶液、NaCl溶液 | ||
| C. | 稀盐酸、稀硝酸 | D. | AgNO3溶液、稀HNO3 |
分析 A.铁离子遇KSCN溶液为血红色;
B.NaOH与氯化铁反应生成红褐色沉淀;
C.二者均与氯化铁不反应;
D.氯化铁与硝酸银反应生成白色沉淀.
解答 解:A.氯化铁与KSCN溶液混合为血红色,氯化铁与KCl溶液混合无现象,可鉴别,故A不选;
B.NaOH与氯化铁反应生成红褐色沉淀,氯化铁与NaCl溶液混合无现象,可鉴别,故B不选;
C.二者均与氯化铁不反应,现象相同,不能鉴别,故C选;
D.氯化铁与硝酸银反应生成白色沉淀,氯化铁与硝酸不反应,可鉴别,故D不选;
故选C.
点评 本题考查物质的鉴别和检验,为高频考点,把握物质的性质、发生的反应及现象为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大.

练习册系列答案
 字词句段篇系列答案
字词句段篇系列答案
相关题目
18.某气态烃0.5mol能与1mol HCl氯化氢完全加成,加成产物分子上的氢原子又可被3mol Cl2取代,则气态烃可能是( )
| A. | CH≡CH | B. | CH2=CH2 | C. | CH2=C(CH3)CH3 | D. | CH≡C-CH3 |
19.有关下图所示化合物的说法不正确的是( )
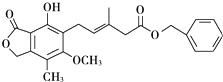

| A. | 1mol该化合物最多可以与3molNaOH反应 | |
| B. | 既可以与Br2的CCl4溶液发生加成反应,又可在光照下与Br2发生取代反应 | |
| C. | 既可以催化加氢,又可以使酸性KMnO4溶液褪色 | |
| D. | 既可以与FeCl3溶液发生显色反应,又可与NaHCO3溶液反应放出CO2气体 |
16. 请根据如表相关信息,回答问题.
请根据如表相关信息,回答问题.
(1)请把B以及B同周期且原子序数比B小的原子按第一电离能从大到小的顺序排列:Mg>Al>Na(用相应的元素符号表示).A、D两种元素中,电负性A>D (填“>”或“<”)
(2)A3分子的空间构型为V形,与其互为等电子体的分子为SO2;
(3)解释在水中的溶解度C7H15OH比乙醇低的原因是:乙醇中的羟基与水的羟基结构相似所以溶解度大,C7H15OH中烃基大,与水的羟基结构相似程度小所以溶解度小,C7H15OH 中采用sp3杂化的原子共有8个;
(4)E(NH3)42+配离子中存在的化学键类型有①③(填序号):
①配位键 ②金属键 ③极性共价键 ④非极性共价键 ⑤离子键 ⑥氢键
若 E(NH3)42+具有对称的空间构型.且当 E(NH3)42+中的两个NH3分子被两个Cl-取代时.能得到两种不同结构的产物,则 E(NH3)42+的空间构型为a(填序号).
a.平面正方形b.正四面体 c.三角锥形 d.V形
(5)单质E晶胞如图所示,已知E元素相对原子质量为M,原子半径为r pm,密度为ρg/cm3 (1pm=10-10cm)那么写出阿伏伽德罗常数NA的表达式$\frac{\sqrt{2}×10{\;}^{30}M}{8ρr{\;}^{3}}$(用M、r、ρ表示).
 请根据如表相关信息,回答问题.
请根据如表相关信息,回答问题.| A | 基态原子最外层电子数是次外层的三倍 |
| B | 基态原子核外有13种不同运动状态的电子 |
| C | 与B同一周期,原子中未成对电子数是同周期中最多 |
| D | D2-的核外电子排布与氩原子相同 |
| E | 是ds区原子序数最小的元素 |
(2)A3分子的空间构型为V形,与其互为等电子体的分子为SO2;
(3)解释在水中的溶解度C7H15OH比乙醇低的原因是:乙醇中的羟基与水的羟基结构相似所以溶解度大,C7H15OH中烃基大,与水的羟基结构相似程度小所以溶解度小,C7H15OH 中采用sp3杂化的原子共有8个;
(4)E(NH3)42+配离子中存在的化学键类型有①③(填序号):
①配位键 ②金属键 ③极性共价键 ④非极性共价键 ⑤离子键 ⑥氢键
若 E(NH3)42+具有对称的空间构型.且当 E(NH3)42+中的两个NH3分子被两个Cl-取代时.能得到两种不同结构的产物,则 E(NH3)42+的空间构型为a(填序号).
a.平面正方形b.正四面体 c.三角锥形 d.V形
(5)单质E晶胞如图所示,已知E元素相对原子质量为M,原子半径为r pm,密度为ρg/cm3 (1pm=10-10cm)那么写出阿伏伽德罗常数NA的表达式$\frac{\sqrt{2}×10{\;}^{30}M}{8ρr{\;}^{3}}$(用M、r、ρ表示).
17.一定质量的某有机物和足量的金属钠反应,可得到Va L气体.向等质量该有机物的溶液中加入足量的Na2CO3溶液,可得到Vb L气体(不考虑气体溶于水),已知在同温同压下Va>Vb,则该有机物可能是( )
| A. | CH3CH(OH)COOH | B. | HO(CH2)2CHO | C. | HOOC-COOH | D. | CH3CH2COOH |
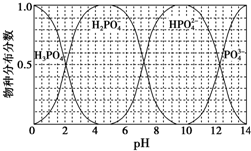 磷的重要化合物NaH2PO4、Na2HPO4和Na3PO4可通过H3PO4与NaOH溶液反应获得,含磷各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH的关系如图所示.
磷的重要化合物NaH2PO4、Na2HPO4和Na3PO4可通过H3PO4与NaOH溶液反应获得,含磷各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH的关系如图所示.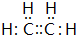 B的结构简式
B的结构简式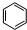 .
. ,反应类型:取代反应.
,反应类型:取代反应.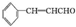 )在自然界存在于桂油中,是一种常用的植物调味油,工业上主要是按如下路线合成的:
)在自然界存在于桂油中,是一种常用的植物调味油,工业上主要是按如下路线合成的: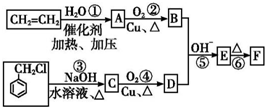

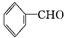 ;检验其中官能团的试剂为银氨溶液或新制的Cu(OH)2悬浊液.
;检验其中官能团的试剂为银氨溶液或新制的Cu(OH)2悬浊液.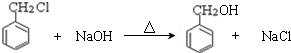 .
.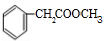 .
.