题目内容
[化学-物质结构与性质]
Ⅰ、为减少温室效应,科学家设计反应:CO2+4H2→CH4+2H2O以减小空气中CO2.
(1)若有1 mol CH4生成,则有________mol σ键和________mol π键断裂.
(2)CH4失去H-(氢负离子)形成CH+3(甲基正离子).已知CH+3的空间结构是平面正三角形,则CH+3中碳原子的杂化方式为________.
Ⅱ、金属原子与CO形成的配合物称为金属羰基配合物(如羰基铁).形成配合物时,每个CO提供一对电子与金属原子形成配位键,且金属原子的价电子和CO提供的电子总和等于18.
(3)金属羰基配合物中,微粒间作用力有________(填字母代号)
a、离子键
b、共价键
c、配位键
d、金属键
(4)羰基铁是一种黄色油状液体,熔点-21℃、沸点102.8℃.由此推测,固体羰基铁更接近于________(填晶体类型).若用Fe(CO)x表示羰基铁的化学式,则x=________.
Ⅲ.研究表明,对于中心离子为Hg2+等阳离子的配合物,若配位体给出电子能力越强:则配位体与中心离子形成的配位键就越强,配合物也就越稳定.
(5)预测HgCl42-与HgI42-的稳定性强弱,并从元素电负性的角度加以解释.
答:HgCl42-比HgI42-更________(填“稳定”或“不稳定”),因为________.
答案:
解析:
解析:
|
(1)6、2(各1分) (2)sp2(2分) (3)bc(2分,各1分) (4)分子晶体 5(各2分) (5)不稳定(1分),Cl电负性大于I,给出电子能力较弱,形成配位键较弱,配合物较不稳定(2分) |

练习册系列答案
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案
相关题目



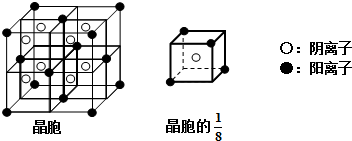
 [化学--选修物质结构与性质]不锈钢以其优异的抗腐蚀性能越来越受到人们的青睐,它主要是由铁、铬、镍、铜、碳等元素所组成的合金.
[化学--选修物质结构与性质]不锈钢以其优异的抗腐蚀性能越来越受到人们的青睐,它主要是由铁、铬、镍、铜、碳等元素所组成的合金.