题目内容
在新制的氯水的各种微粒中:(用化学式或离子符号填写)
(1)使氯水呈浅黄绿色的是
(2)能使紫色石蕊试液显红色的是
(3)能使湿润红纸褪色的是
(4)能使无水硫酸铜变蓝的是
(5)能使AgNO3溶液产生白色沉淀的是
(6)能与NaHCO3反应放出气体的是 .
(1)使氯水呈浅黄绿色的是
(2)能使紫色石蕊试液显红色的是
(3)能使湿润红纸褪色的是
(4)能使无水硫酸铜变蓝的是
(5)能使AgNO3溶液产生白色沉淀的是
(6)能与NaHCO3反应放出气体的是
考点:氯气的化学性质
专题:元素及其化合物
分析:氯气溶于水,在水中发生Cl2+H2O?H++Cl-+HClO,HClO为若电解质,则溶液中存在的分子有H2O、Cl2、HClO等,存在的离子有:H+、Cl-、OH-、ClO-等,根据微粒的性质来回答.
解答:
解:(1)氯气是黄绿色气体,氯水中存在化学平衡,CL2+H2O=HCl+HClO,溶液中存在氯气分子呈黄绿色,故答案为:Cl2;
(2)能使紫色石蕊试液显红色的是H+,故答案为:H+;
(3)能使湿润的红纸褪色的是HClO,故答案为:HClO;
(4)能使无水硫酸铜变蓝的是H2O,故答案为:H2O;
(5)滴加AgNO3溶液后生成白色沉淀,是盐酸电离的氯离子和银离子反应生成氯化银沉淀,Ag++Cl-=AgCl↓,故答案为:Cl-或HCl;
(6)能与碳酸氢钠溶液反应放出气体的是H+,故答案为:H+或HCl.
(2)能使紫色石蕊试液显红色的是H+,故答案为:H+;
(3)能使湿润的红纸褪色的是HClO,故答案为:HClO;
(4)能使无水硫酸铜变蓝的是H2O,故答案为:H2O;
(5)滴加AgNO3溶液后生成白色沉淀,是盐酸电离的氯离子和银离子反应生成氯化银沉淀,Ag++Cl-=AgCl↓,故答案为:Cl-或HCl;
(6)能与碳酸氢钠溶液反应放出气体的是H+,故答案为:H+或HCl.
点评:本题考查氯水成分,为高频考点,侧重于元素化合物知识的综合理解和运用的考查,题目难度不大,本题注意把握氯气与水反应的性质以及次氯酸的性质.

练习册系列答案
相关题目
一支规格为AmL的酸式滴定管,其尖咀部分充满液体时,液面在mmL刻度处,当液面降低到nmL刻度处时,下列判断正确的是( )
| A、流出的流体的体积是(m-n)mL |
| B、流出的液体的体积是(n-m)mL |
| C、滴定管内剩余的液体的体积是(A-n)mL |
| D、滴定管内剩余的液体的体积大于(A-n)mL |
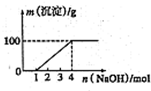 某澄清透明溶液中只可能含有①Al3+;②Mg2+;③Fe3+;④Fe2+;⑤H+;⑥CO32-;⑦NO3-中的几种,向该溶液中逐滴加入NaOH溶液至过量,生成沉淀的质量与NaOH的物质的量的关系如图所示.则该溶液中一定含有的离子是( )
某澄清透明溶液中只可能含有①Al3+;②Mg2+;③Fe3+;④Fe2+;⑤H+;⑥CO32-;⑦NO3-中的几种,向该溶液中逐滴加入NaOH溶液至过量,生成沉淀的质量与NaOH的物质的量的关系如图所示.则该溶液中一定含有的离子是( )| A、③⑤⑦ | B、②③⑤⑦ |
| C、①②③⑥⑦ | D、①②③④⑤⑦ |
下列变化不可能通过一步实验直接完成的是( )
| A、Al(OH)3→Al2O3 |
| B、Al2O3→Al(OH)3 |
| C、Al→AlO2- |
| D、AlCl3→Al(OH)3 |
下列反应最终能生成Fe3+的化合物的是( )
①过量Fe与HNO3
②铁丝在硫蒸汽中燃烧
③向FeBr2溶液中通入Cl2
④铁与CuCl2溶液反应
⑤Fe(OH)2露置于空气中.
①过量Fe与HNO3
②铁丝在硫蒸汽中燃烧
③向FeBr2溶液中通入Cl2
④铁与CuCl2溶液反应
⑤Fe(OH)2露置于空气中.
| A、①②③ | B、①③⑤ |
| C、③④ | D、③⑤ |
以石墨为电极,电解KI溶液(含有少量的酚酞和淀粉),下列说法错误的是( )
| A、阴极附近溶液呈红色 |
| B、阴极反应式与硫酸钠溶液时相同 |
| C、阳极附近溶液呈蓝色 |
| D、溶液的pH变小 |
 100mL某无色溶液由H+、Na+、Mg2+、Al3+、Fe3+、CO32-、Cl-等离子中的几种混合组成(不考虑水电离出的离子),向溶液中逐滴加0.5mol/L氢氧化钠溶液直到过量,产生沉淀的情况如图所示.
100mL某无色溶液由H+、Na+、Mg2+、Al3+、Fe3+、CO32-、Cl-等离子中的几种混合组成(不考虑水电离出的离子),向溶液中逐滴加0.5mol/L氢氧化钠溶液直到过量,产生沉淀的情况如图所示.