题目内容
5.下列叙述正确的是( )| A. | 在原电池的负极和电解池的阴极上都是发生失电子的氧化反应 | |
| B. | 用惰性电极精炼铜时,电解质溶液没有变化 | |
| C. | 用惰性电极电解饱和NaCl溶液,若有1 mol电子转移,则生成1 molNaOH | |
| D. | 镀层破损后,镀锡铁板比镀锌铁板更耐腐蚀 |
分析 A、原电池中负极失电子和电解池的阳极发生氧化反应;
B、电解精炼时,根据阴阳极上铜的质量变化判断溶液中铜离子浓度是否变化;
C、用惰性电极电解饱和NaCl溶液,发生2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑;
D、铁、锡和合适的电解质溶液构成的原电池中,铁作负极,易被腐蚀,锌、铁和合适的电解质溶液构成的原电池中,锌作负极,铁作正极被保护.
解答 解:A、原电池中负极失电子和电解池的阳极发生氧化反应,而不是电解池的阴极,故A错误;
B、电解精炼铜时,阳极上溶解的金属不仅有铜还有其它金属,阴极上只析出铜,所以溶解的铜小于析出的铜,导致溶液中铜离子浓度减小,故B错误;
C、用惰性电极电解饱和NaCl溶液,发生2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑,若有1mol电子转移,则生成1mol NaOH,故C正确;
D镀层破损后,镀锡铁板中铁加快腐蚀,镀锌铁板中铁被保护,所以镀锌铁板比镀锡铁板更耐腐蚀,故D错误;
故选C.
点评 本题考查原电池和电解池的工作原理,为高考常见题型,注意把握工作原理和离子的放电顺序,题目难度中等.

练习册系列答案
相关题目
15.下列化学反应,能用离子方程式H++OH-═H2O来表示的是( )
| A. | 盐酸和氢氧化铜 | B. | 硫酸和氢氧化钠溶液 | ||
| C. | 醋酸和氢氧化钡溶液 | D. | 稀硝酸和氨水混合 |
16.胶体区别于其他分散系的本质特征是( )
| A. | 分散质粒子能做不停的,无规则的运动 | |
| B. | 是否有丁达尔现象 | |
| C. | 静置后既不分层,也无沉淀产生 | |
| D. | 分散质粒子直径在10-7-10-9m之间 |
10.用活性炭还原法处理氮氧化物.有关反应为C(s)+2NO(g)?N2(g)+CO2(g).某研究小组向恒容密闭容器中加入一定量的活性炭和NO,恒温(T℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
(1)10~20min以v(CO2)表示的反应速率为0.009 mol•L-1•min-1.
(2)根据表中数据,计算T℃时该反应的平衡常数为0.56(保留两位小数).
(3)下列各项能作为判断该反应达到平衡标志的是CD(填序号字母).
A.容器内压强保持不变 B.2v正(NO)=v逆(N2)
C.容器内CO2的体积分数不变 D.混合气体的密度保持不变
(4)30min时改变某一条件,反应重新达到平衡,则改变的条件可能是分离出了二氧化碳(减小CO2的浓度).
(5)一定温度下,随着NO的起始浓度增大,则NO的平衡转化率不变(填“增大”“不变”或“减小”).
| 物质浓度(mol/L)时间(min) | NO | N2 | CO2 |
| 0 | 1.00 | 0 | 0 |
| 10 | 0.58 | 0.21 | 0.21 |
| 20 | 0.40 | 0.30 | 0.30 |
| 30 | 0.40 | 0.30 | 0.30 |
| 40 | 0.32 | 0.34 | 0.17 |
| 50 | 0.32 | 0.34 | 0.17 |
(2)根据表中数据,计算T℃时该反应的平衡常数为0.56(保留两位小数).
(3)下列各项能作为判断该反应达到平衡标志的是CD(填序号字母).
A.容器内压强保持不变 B.2v正(NO)=v逆(N2)
C.容器内CO2的体积分数不变 D.混合气体的密度保持不变
(4)30min时改变某一条件,反应重新达到平衡,则改变的条件可能是分离出了二氧化碳(减小CO2的浓度).
(5)一定温度下,随着NO的起始浓度增大,则NO的平衡转化率不变(填“增大”“不变”或“减小”).
17.某种中和胃酸的药物主要成分的化学式为Al2Mg6(OH)16CO3•4H2O.1molAl2Mg6(OH)16CO3•4H2O中,氧原子的物质的量为( )
| A. | 16mo1 | B. | 19 mol | C. | 20mol | D. | 23mol |
3.下列说法正确的是( )
| A. | 按系统命名法,化合物 的名称是2,5,5-三甲基-3-乙基庚烷 的名称是2,5,5-三甲基-3-乙基庚烷 | |
| B. | 将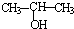 与NaOH的醇溶液共热可制备CH3-CH═CH2 与NaOH的醇溶液共热可制备CH3-CH═CH2 | |
| C. | 向柠檬醛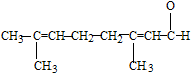 中加入酸性高锰酸钾,若溶液褪色,说明分子中含有醛基 中加入酸性高锰酸钾,若溶液褪色,说明分子中含有醛基 | |
| D. | 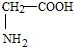 、 、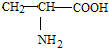 、 、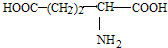 三种氨基酸脱水,最多可生成6种二肽 三种氨基酸脱水,最多可生成6种二肽 |
4.X、Y、Z是三种短周期元素,其中X、Y位于同一主族,Y、Z处于同一周期.X原子的最外层电子数是其电子层数的3倍.Z原子的核外电子数比Y原子少l.下列说法正确的是( )
| A. | 三种元素的氢化物中只有极性键没有非极性键 | |
| B. | Y元素最高价氧化物对应水化物的化学式可表示为H3YO4 | |
| C. | 三种元素的气态最简单氢化物中Z的氢化物最稳定 | |
| D. | 原子半径由大到小的顺序为Z>Y>X |