题目内容
下列电子式正确的是( )
A、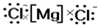 |
B、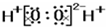 |
C、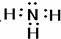 |
D、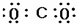 |
考点:电子式
专题:化学键与晶体结构
分析:A.氯化镁为离子化合物,镁离子应该标出电荷,氯离子应该用中括号;
B.过氧化氢为共价化合物,分子中不存在阴阳离子;
C.氨气分子中存在3个氮氢键,氮原子最外层达到8电子稳定结构;
D.二氧化碳分子中存在两个碳氧双键.
B.过氧化氢为共价化合物,分子中不存在阴阳离子;
C.氨气分子中存在3个氮氢键,氮原子最外层达到8电子稳定结构;
D.二氧化碳分子中存在两个碳氧双键.
解答:
解:A.氯化镁属于离子化合物,阴阳离子都需要标出所带电荷,阴离子还需要标出最外层电子,氯化镁正确的电子式为: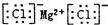 ,故A错误;
,故A错误;
B.过氧化氢分子中不存在阴阳离子,不能标出阴阳离子的电荷,其正确的电子式为: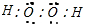 ,故B错误;
,故B错误;
C.氨气为共价化合物,分子中存在3个氮氢键,氮原子最外层达到8电子,氨气的电子式为: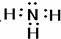 ,故C正确;
,故C正确;
D.二氧化碳为共价化合物,分子中存在两个碳氧双键,二氧化碳正确的电子式为: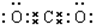 ,故D错误;
,故D错误;
故选C.
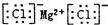 ,故A错误;
,故A错误;B.过氧化氢分子中不存在阴阳离子,不能标出阴阳离子的电荷,其正确的电子式为:
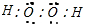 ,故B错误;
,故B错误;C.氨气为共价化合物,分子中存在3个氮氢键,氮原子最外层达到8电子,氨气的电子式为:
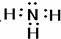 ,故C正确;
,故C正确;D.二氧化碳为共价化合物,分子中存在两个碳氧双键,二氧化碳正确的电子式为:
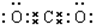 ,故D错误;
,故D错误;故选C.
点评:本题考查了电子式的书写判断,题目难度中等,注意掌握电子式的概念及正确书写方法,明确原子、分子、阴阳离子的电子式的区别,试题培养了学生灵活应用所学知识的能力.

练习册系列答案
相关题目
根据电子排布的特点,铜元素在周期表属于( )
| A、s区 | B、p区 |
| C、d 区 | D、ds区 |
某元素原子核外L层电子数是其它层电子数之和的2倍,则该元素的核电荷数为( )
| A、7 | B、8 | C、12 | D、16 |
 已知NO2和N2O4可以相互转化:2NO2(g)?N2O4(g)△H<0.现将一定量NO2和N2O4的混合气体通入体积为1L的恒温密闭容器中,反应物浓度随时间变化关系如图.下列说法错误的是( )
已知NO2和N2O4可以相互转化:2NO2(g)?N2O4(g)△H<0.现将一定量NO2和N2O4的混合气体通入体积为1L的恒温密闭容器中,反应物浓度随时间变化关系如图.下列说法错误的是( )| A、图中共有两条曲线X和Y,其中曲线X表示NO2浓度随时间的变化 |
| B、a、b、c、d四个点中,表示化学反应处于平衡状态的点是b和d |
| C、反应进行至25min时,曲线发生变化的原因是加入0.4mol N2O4 |
| D、若要达到与d相同的状态,在25min时还可以采取的措施是适当缩小容器体积 |
将0.1mol/L的K2SO4溶液、0.2mol/L的Al2(SO4)3溶液和纯水混合,要使混合液中的K+、Al3+、SO42-的浓度分别为0.1mol/L、0.1mol/L、0.2mol/L,则所取的K2SO4溶液、Al2(SO4)3溶液、纯水三者体积比( )
| A、1:1:1 |
| B、2:1:2 |
| C、1:1:2 |
| D、2:1:1 |
下列描述中不符合生产实际的是( )
| A、电解水制氢气时,用铜作阳极 |
| B、电解法精炼粗铜,用纯铜作阴极 |
| C、电解饱和食盐水制烧碱,用涂镍碳钢网作阴极 |
| D、在镀件上电镀锌,用锌作阳极 |
下列气体溶解于水时,发生了氧化还原反应的是( )
| A、SO3溶于水 |
| B、NH3溶于水 |
| C、CO2溶于水 |
| D、NO2溶于水 |
下列过程要吸收热量的是( )
A、 |
B、 |
| C、H++OH-→H2O |
| D、C+O2→CO2 |
X元素最高价氧化物对应的水化物为HnXO2n,则它对应的气态氢化物为( )
| A、H3n-8X |
| B、H3nX |
| C、H8-3nX |
| D、H12-3nX |