题目内容
下列过程要吸收热量的是( )
A、 |
B、 |
| C、H++OH-→H2O |
| D、C+O2→CO2 |
考点:吸热反应和放热反应
专题:化学反应中的能量变化
分析:断键吸收能量,成键放出能量;
常见的放热反应有:所有的物质燃烧、所有金属与酸、所有中和反应;绝大多数化合反应、置换反应;少数分解、复分解反应;常见的吸热反应有:个别的化合反应(如C和CO2),绝大数分解反应,少数分解置换以及某些复分解(如铵盐和强碱).
常见的放热反应有:所有的物质燃烧、所有金属与酸、所有中和反应;绝大多数化合反应、置换反应;少数分解、复分解反应;常见的吸热反应有:个别的化合反应(如C和CO2),绝大数分解反应,少数分解置换以及某些复分解(如铵盐和强碱).
解答:
解:A.断键吸收能量,故A正确;
B.成键放出能量,故B错误;
C.中和反应是放热反应,故C错误;
D.碳与氧气的反应是放热反应,故D错误.
故选A.
B.成键放出能量,故B错误;
C.中和反应是放热反应,故C错误;
D.碳与氧气的反应是放热反应,故D错误.
故选A.
点评:本题考查吸热反应和放热反应,难度不大,比较基础,侧重对基础知识的巩固,注意对基础知识的理解掌握.

练习册系列答案
相关题目
鉴别NO2气体和Br2蒸气,可用 ( )
①湿润的淀粉KI试纸 ②AgNO3溶液 ③水 ④烧碱溶液.
①湿润的淀粉KI试纸 ②AgNO3溶液 ③水 ④烧碱溶液.
| A、①④ | B、③④ | C、②③ | D、全部 |
下列电子式正确的是( )
A、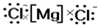 |
B、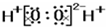 |
C、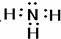 |
D、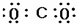 |
下列关于原电池的叙述中,正确的是( )
| A、负极发生的电极反应是还原反应 |
| B、电极只能由两种不同的金属构成 |
| C、工作时其正极不断产生电子并经外电路流向负极 |
| D、能将化学能转变为电能 |
下列化合物中,含有非极性共价键的离子化合物是( )
| A、CaC2 |
| B、N2H4 |
| C、Na2S |
| D、NH4NO3 |
科学家制造出由4个氧原子构成的氧分子,并用质谱仪探测后证实了它的存在.若该氧分子具有空间对称结构,下列关于该氧分子的说法正确的是( )
| A、是氧元素的一种同位素 |
| B、是氧气的同素异形体,分子内含有共价键 |
| C、是一种新的氧化物 |
| D、是臭氧的同分异构体 |
金属钠是一种活泼金属,除了具有金属的一般性质外,还具有自己的特性.关于钠的叙述中,正确的是( )
| A、钠是银白色金属,熔点低,硬度大 |
| B、钠放置在空气中,会迅速被氧化而生成淡黄色的氧化钠 |
| C、加热时,金属钠剧烈燃烧,产生黄色火焰 |
| D、金属钠着火可以用泡沫灭火器或用干燥的沙土灭火 |
已知2H2(g)+O2(g)→2H2O(g)+483.6kJ.下列说法或表达正确的是( )
| A、在相同的条件下,2mol 氢气与1mol氧气的总能量小于2mol水蒸气的总能量 | ||
B、H2(g)+
| ||
C、H2(g)+
| ||
| D、任何条件下,2L水蒸气分解成2L氢气与1L氧气需吸收483.6kJ热量 |
下列关于离子化合物的叙述正确的是( )
| A、离子化合物中都含有离子键 |
| B、离子化合物中的阳离子只能是金属离子 |
| C、离子化合物如能溶于水,其水溶液一定可以导电 |
| D、溶于水可以导电的化合物一定是离子化合物 |