题目内容
20.NA表示阿伏伽德罗常数的数值,下列说法正确的是( )| A. | 标准状况下22.4L任意比的氢气和二氧化碳的混合气体中含有的分子总数均为NA | |
| B. | 0.1mol/LNaCl溶液中Na+的数目为0.1NA | |
| C. | 标准状况下,5.6L四氯化碳含有的分子数为0.25NA | |
| D. | 500mL0.2mol/L饱和FeCl3溶液完全转化可制得0.1NA个Fe(OH)3胶粒 |
分析 A、求出混合气体的物质的量,然后根据1mol任何气体中含NA个分子来分析;
B、溶液体积不明确,不能计算微粒数;
C、标况下四氯化碳为液态,标准状况气体摩尔体积为22.4L/mol;
D.氢氧化铁胶体微粒是氢氧化铁的集合体;
解答 解:A、标况下22.4L混合气体的物质的量=$\frac{22.4L}{22.4L/mol}$=1mol,而1mol任何气体中含NA个分子,标准状况下22.4L任意比的氢气和二氧化碳的混合气体中含有的分子总数均为NA,故A正确;
B、溶液体积不明确,故溶液中的钠离子的个数无法计算,故B错误;
C、标况下四氯化碳为液态,故不能根据气体摩尔体积来计算其物质的量,故C错误;
D.一个氢氧化铁胶粒是多个氢氧化铁的集合体,故得到的氢氧化铁胶粒的个数小于0.1NA个,故D错误;
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度中等.

练习册系列答案
相关题目
8.下列生活常识与化学原理有关,正确的选项是( )
①福尔马林具有防腐杀菌的作用,是因为甲醛可以使蛋白质变性
②人体血液pH保持弱碱性(7.35~7.45),主要是血液中存在HCO3-
③硫酸亚铁补铁剂应与维生素C同服,是因为维生素C可以防止Fe2+被氧化
④油炸食品容易产生“哈喇”味而不能食用,是因为被氧化.
①福尔马林具有防腐杀菌的作用,是因为甲醛可以使蛋白质变性
②人体血液pH保持弱碱性(7.35~7.45),主要是血液中存在HCO3-
③硫酸亚铁补铁剂应与维生素C同服,是因为维生素C可以防止Fe2+被氧化
④油炸食品容易产生“哈喇”味而不能食用,是因为被氧化.
| A. | ①②③④ | B. | ①②③ | C. | ②③④ | D. | ①③④ |
15.下列有关物质用途的说法中,不正确的是( )
| A. | 硅胶可作为袋装食品的干燥剂 | B. | 氨气是生产硝酸的主要原料 | ||
| C. | Fe3O4可用于制备红色油漆、涂料 | D. | NH4HCO3可用作化肥 |
5.在我们的日常生活中出现了的“增铁酱油”,这里的铁应理解为( )
| A. | 铁的氢氧化物 | B. | 铁的氧化物 | C. | 铁元素 | D. | 铁屑 |
12.某天然碱的化学式可表示为3Na2CO3•NaHCO3•2H2O,取少量该物质溶于水得稀溶液,在溶液中逐滴滴加稀盐酸.下列离子方程式与事实不相符的是( )
| A. | HCO3-+CO32-+3H+→2CO2↑+2H2O | B. | HCO3-+3CO32-+7H+→4CO2↑+4H2O | ||
| C. | 2HCO3-+CO32-+4H+→3CO2↑+3H2O | D. | CO32-+H+→HCO3- |
9.在反应X+2Y═2R+M中,已知R和M的摩尔质量之比为22:9,当1.7g X与Y完全反应后,生成4.4g R.则在此反应中Y和R的质量之比为( )
| A. | 16:9 | B. | 9:11 | C. | 32:9 | D. | 46:9 |
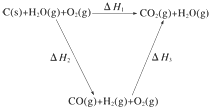 将煤转化为水煤气的主要化学反应为C(s)+H2O(g)$\frac{\underline{\;高温\;}}{\;}$CO(g)+H2(g);
将煤转化为水煤气的主要化学反应为C(s)+H2O(g)$\frac{\underline{\;高温\;}}{\;}$CO(g)+H2(g);