题目内容
某同学利用如图所示装置探究金属的腐蚀与防护条件.下列说法不合理的是( )

| A、①区Cu电极上产生气泡,Fe电极附近滴加K3[Fe(CN)6]后出现蓝色,Fe被腐蚀 |
| B、②区Cu电极附近滴加酚酞后变成红色,Fe电极附近滴加K3[Fe(CN)6]出现蓝色,Fe被腐蚀 |
| C、③区Zn电极反应式为Zn-2e-═Zn2+,Fe电极附近滴加K3[Fe(CN)6]未出现蓝色,Fe被保护 |
| D、④区Zn电极反应式为2H++2e-═H2↑,Fe电极附近滴加K3[Fe(CN)6]出现蓝色,Fe被腐蚀 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:①为原电池,Fe为负极,发生氧化反应,②为电解装置,Fe为阳极,③为原电池,Fe为正极,④为电解装置,Fe为阳极,结合电极反应解答该题.
解答:
解:A.①为原电池,Fe为负极,发生吸氧腐蚀,没有气体生成,故A错误;
B.②区Cu电极为阴极,生成氢气和氢氧化钠,Cu电极附近滴加酚酞后变成红色,Fe为阳极,被氧化生成亚铁离子,滴加K3[Fe(CN)6]出现蓝色,故B正确;
C.③为原电池,Fe为正极,Zn被氧化,电极方程式为Zn-2e-═Zn2+,故C正确;
D.④为电解装置,Fe为阳极,被氧化生成亚铁离子,滴加K3[Fe(CN)6]出现蓝色,Zn电极为阴极,反应式为2H++2e-═H2↑,故D正确.
故选A.
B.②区Cu电极为阴极,生成氢气和氢氧化钠,Cu电极附近滴加酚酞后变成红色,Fe为阳极,被氧化生成亚铁离子,滴加K3[Fe(CN)6]出现蓝色,故B正确;
C.③为原电池,Fe为正极,Zn被氧化,电极方程式为Zn-2e-═Zn2+,故C正确;
D.④为电解装置,Fe为阳极,被氧化生成亚铁离子,滴加K3[Fe(CN)6]出现蓝色,Zn电极为阴极,反应式为2H++2e-═H2↑,故D正确.
故选A.
点评:本题考查了原电池原理和电解池原理的应用,为高频考点,侧重于学生的分析能力的考查,题目难度不大,注意把握电极的判断和电极方程式的书写.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列化学用语表示正确的是( )
A、S2-的离子结构示意图: |
| B、次氯酸的结构式:H-O-Cl |
C、水分子的比例模型: |
D、NCl3的电子式: |
化学与生产、生活、环境密切相关,下列有关说法正确的是( )
| A、半导体行业中有一句话:“从沙滩到用户”,计算机芯片的材料是二氧化硅 |
| B、“地沟油”经过加工处理后,可以用来制肥皂和生物柴油 |
| C、食品包装袋中常放入小袋的生石灰,目的是防止食品氧化变质 |
| D、二氧化硫的大量排放是造成光化学烟雾的主要原因 |
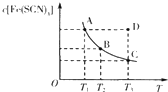 已知:FeCl3(aq)+3KSCN(aq)?3KCl(aq)+Fe(SCN)3(aq),平衡时Fe(SCN)3的物质的量浓度与温度T的关系如图所示,则下列说法正确的是( )
已知:FeCl3(aq)+3KSCN(aq)?3KCl(aq)+Fe(SCN)3(aq),平衡时Fe(SCN)3的物质的量浓度与温度T的关系如图所示,则下列说法正确的是( )| A、A点与B点相比,A点的c( Fe3+)大 |
| B、加入KCl固体可以使溶液由D点变到C点 |
| C、反应处于D点时,一定有υ(正)<υ(逆) |
| D、若T1、T2温度下的平衡常数分别为K1、K2,则K1<K2 |
化学与生产、生活、坏境保护等密切相关.下列说法正确的是( )
| A、“辽宁舰”上用于舰载机降落拦阻索的特种钢缆属于新型无机非金属材料 |
| B、能够改善饮品的色、香、味,并有防腐保鲜作用的食品添加剂应限量使用 |
| C、雾霾是由大量的燃烧煤、石油、天然气等产生的二氧化碳含量偏高所致 |
| D、煤的主要成分为单质碳、苯、二甲苯等,可通过煤的干馏将它们分离 |
 X、Y、Z、W均为短周期元素,它们在元素周期表中相对位置如图所示,若Z原子的最外层电子数是第一层电子数的3倍,下列说法正确的是( )
X、Y、Z、W均为短周期元素,它们在元素周期表中相对位置如图所示,若Z原子的最外层电子数是第一层电子数的3倍,下列说法正确的是( )| A、Z单质与氢气反应较Y剧烈 |
| B、X与W的原子核外电子数相差9 |
| C、X单质氧化性强于Y单质 |
| D、最高价氧化物对应水化物酸性W比Z强 |
只有在化合物中才能存在的化学键是( )
| A、离子键 | B、共价键 |
| C、极性键 | D、非极性键 |
 已知水在25℃和95℃时,其电离平衡曲线如图所示.
已知水在25℃和95℃时,其电离平衡曲线如图所示. 现有W、A、B、C、D、E、F七种前四周期元素,原子序数依次增大.目前公认W、A都各自形成的化合物种类最多.A、B、C位于同周期且第一电离能按A、C、B的顺序依次增大.D、E位于同主族,且D的原子序数为12.F的单质为紫红色常见金属.请回答下列问题:
现有W、A、B、C、D、E、F七种前四周期元素,原子序数依次增大.目前公认W、A都各自形成的化合物种类最多.A、B、C位于同周期且第一电离能按A、C、B的顺序依次增大.D、E位于同主族,且D的原子序数为12.F的单质为紫红色常见金属.请回答下列问题: